L50 Крапивница, МКБ-10
- L50.0 Аллергическая крапивница
- L50.1 Идиопатическая крапивница
- L50.2 Крапивница, вызванная воздействием низкой или высокой температуры
- L50.3 Дерматографическая крапивница
- L50.4 Вибрационная крапивница
- L50.5 Холинергическая крапивница
- L50.6 Контактная крапивница
- L50.8 Другая крапивница
- L50.9 Крапивница неуточненная
Отредактировано: 05.07.2024
Крапивница
Определение и классификация
Крапивница (от лат. Urtica – крапива) – группа заболеваний, характеризующихся развитием волдырей, ангиоотеков или обоих проявлений вместе. Существует ряд состояний, не относящихся к крапивнице, при которых волдыри не являются ведущим симптомом (например, аутовоспалительные синдромы, анафилаксия, уртикарный васкулит, наследственный ангиоотек (НАО)) [1].
По длительности течения крапивница подразделяется на острую (продолжительность появления волдырей до 6 недель) и хроническую (непрерывное появление волдырей в течение 6 недель и более). Хроническая крапивница включает подтипы в зависимости от особенностей патогенеза и провоцирующего фактора:
- Хроническая спонтанная крапивница (ХСК) – наиболее распространенный подтип хронической крапивницы. Диагностируется, если не удается определить конкретный фактор, провоцирующий появление волдырей.
- Хроническая индуцированная крапивница
- Физическая крапивница:
- симптоматический дермографизм,
- индуцируемая холодом крапивница,
- индуцируемая теплом крапивница,
- солнечная крапивница,
- отсроченная крапивница от давления,
- вибрационный ангиоотек,
- Другие индуцируемые крапивницы:
- холинергическая крапивница,
- контактная крапивница,
- аквагенная крапивница.
Этиология и патогенез
Крапивница – заболевание, обусловленное избыточной дегрануляцией тучных клеток, провоцируемой экзо- и эндогенными факторами. Гистамин и другие медиаторы, такие как фактор активации тромбоцитов и высвобождаемые активированными тучными клетками цитокины приводят к активации чувствительных нервных окончаний, расширению сосудов и экстравазации плазмы, а также к рекрутированию клеток в очаги поражения. Гистологически волдыри характеризуются отеком верхних и средних слоев дермы с увеличением проницаемости и расширением посткапиллярных венул, а также лимфатических сосудов верхних слоев дермы, что приводит к истечению плазмы крови в ткани. При ангионевротическом отеке аналогичные изменения происходят преимущественно в нижних слоях дермы и подкожном слое [2].
Ни одна из теорий патогенеза крапивницы не была полностью доказана. К наиболее описанным гипотезам относятся аутоиммунная теория, теории, связанные с гистамин-высвобождающими факторами, и теория клеточных дефектов.
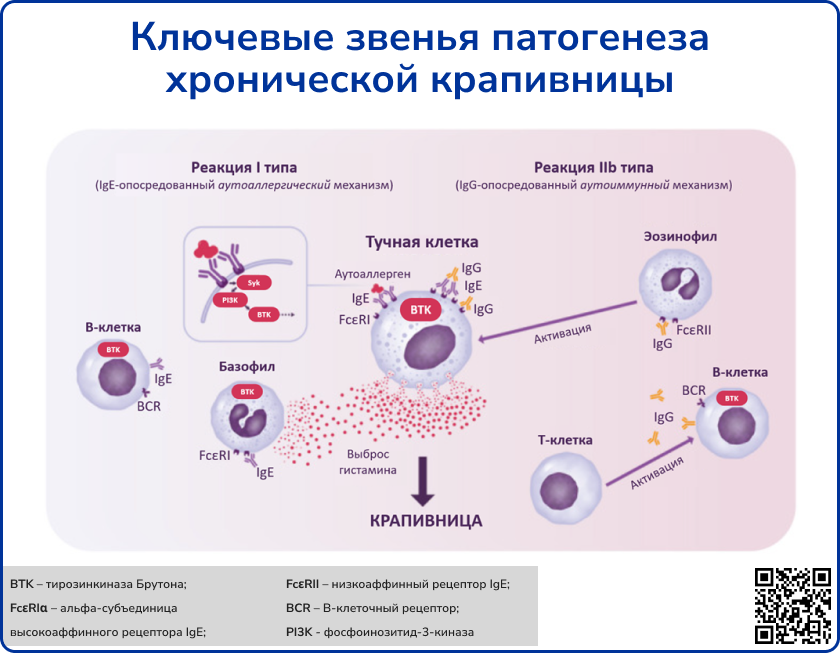
Источник: Mendes‐Bastos P. et al. Bruton's tyrosine kinase inhibition—An emerging therapeutic strategy in immune‐mediated dermatological conditions //Allergy. – 2022. – Т. 77. – №. 8. – С. 2355-2366.
Аутоиммунная теория
Концепция о том, что крапивница представляет из себя аутоиммунное расстройство, возникла из-за выявляемости у таких пациентов повышенных титров аутоантител к тканевым компонентам щитовидной железы и связанных с ними нарушений функции органа [3, 4]. Используемый в клинической практике метод диагностики – кожный тест с аутологичной сывороткой (КТАС) – также подтверждает жизнеспособность этой гипотезы. Метод заключается в анализе in vivo активации тучных клеток, индуцированной факторами, содержащимися в сыворотке крови пациента. Сыворотки пациентов с ХСК и положительными КТАС способны вызывать высвобождение гистамина in vitro из базофилов, полученных от контрольных лиц [5]. Поэтому было высказано предположение, что в сыворотке больных присутствуют аутоантитела или другие гистамин-высвобождающие факторы, главные претенденты среди которых – IgG против альфа-субъединицы высокоаффинного рецептора IgE (анти-FcεRIα) и IgG против Fc-области IgE (анти-IgE).
Однако ни положительный кожный тест, ни аутоантитела не являются специфичными для пациентов с крапивницей: аналогичный результат встречается при неаллергической астме, рините, аутоиммунных заболеваниях (системной красной волчанке, дерматомиозите и др.), а также у здоровых лиц [6]. Кроме того, уровень аутоантител при хронической крапивнице не изменяется в зависимости от клинической активности заболевания [7], и их наличие не прогнозирует резистентность к терапии [8].
Теории, связанные с другими факторами сыворотки или плазмы крови
Для выявления веществ, потенциально повышающих проницаемость сосудистой стенки у больных с крапивницей, был проведен ряд исследований с сыворотками пациентов и здоровых лиц (контрольная группа). Хотя сыворотки обеих групп сами по себе не повышали проницаемость эндотелиальных клеток, большинство образцов от больных вызывали дегрануляцию тучных клеток при инкубации с их линиями, одна из которых не имела рецепторов IgE. Супернатанты активированных культур тучных клеток повышали проницаемость эндотелия. Это свойство сохранялось при обеднении сывороток по IgG и не было связано со способностью вызывать положительный КТАС [9].
Состояние многих пациентов с ХСК улучшается на фоне анти-IgE терапии (омализумаб), что позволяет предположить присутствие в организме аномального IgE, который распознает неизвестный антиген или антигены и активирует тучные клетки и базофилы. Таким образом, не исключено, что существуют люди с IgE против аутоантигенов, но данные в пользу этой концепции ограничены.
У некоторых пациентов с хронической идиопатической крапивницей наблюдается избыточная или аномальная продукция тромбоцитарных факторов свертывания, таких как тромбин [10, 11], а также более высокие уровни полипептида F1+2 (образуется при активации протромбина в тромбин), коррелирующие с тяжелым течением крапивницы [10]. Тромбин сам по себе способен активировать тучные клетки и базофилы, повышать проницаемость кровеносных сосудов [12, 13], а также стимулировать выработку C5a, который усиливает IgG-зависимое высвобождение гистамина тучными клетками [14]. Соответственно, у таких пациентов также выявлялись отклонения в системе свертывания крови, которые коррелировали с тяжестью заболевания [15].
Вывод о том, что при хронической крапивнице избыточно активируется внешний путь свертывания крови, согласуется с сообщениями об успешном лечении варфарином в небольшом двойном слепом контролируемом исследовании, а также с описанием случаев пациентов с ХСК, резистентных к антигистаминным препаратам [16, 17].
Теория клеточных дефектов
Теория клеточных дефектов предполагает, что у пациентов с крапивницей нарушены процессы миграции, передачи сигналов или функции тучных клеток и базофилов. Наблюдения, подтверждающие эту концепцию:
- Несмотря на нормальное количество тучных клеток в коже пациентов, дегрануляция при воздействии неиммуногенных соединений (например, соединения 48/80, кодеинсульфата) происходит быстрее, чем у здоровых людей [18]. В том числе это возникает при повышении числа рецепторов к этим соединениям, например, MrgX2 – рецепторов для 48/80 [19].
- Количество базофилов в периферической крови у пациентов с ХСК низкое, особенно при тяжелом течении заболевания, что объясняется их повышенной миграцией в кожу [20].
- В экспериментах высвобождение гистамина снижалось после активации in vitro через FcεRI, но не через другие рецепторы [21, 22]. На основании ряда исследований было выявлено несколько фенотипов базофилов: фенотип с нормальным ответом на активацию FcεRI («ответчики») и фенотип, не отвечающий на IgE-опосредованную активацию («неответчики») и характеризующийся повышенным уровнем внутриклеточных регуляторных белков, ингибирующих сигнальные пути FcεRI. У здоровых людей доля «неответчиков» составляет 10-15% от общего количества базофилов, у пациентов с ХСК оба фенотипа клеток содержатся в равном соотношении.
- У пациентов с тяжелым течением хронической крапивницы помимо повышения доли базофилов-«неответчиков» также наблюдались [23]:
- наличие преактивированных базофилов, которые не могут быть далее активированы стимуляцией FcεRI,
- сниженная поверхностная экспрессия FcεRI и FcγRII,
- сниженное связывание IgE и IgG,
- базопения периферической крови.
Другие теории
Теории об инфекционных агентах и пищевых добавках (псевдоаллергенах) как потенциальных триггерах высыпаний при крапивнице до сих пор активно обсуждаются, несмотря на то что подтверждающие их данные немногочисленны и несистематизированы. Не исключено, что источники хронического воспаления способны предрасполагать восприимчивых пациентов к развитию хронической крапивницы [24].
Инфекционные агенты
Были предприняты попытки связать некоторые распространенные хронические инфекции с ХСК, включая Anisakis simplex [25], Helicobacter pylori [26], вирус гепатита А [27] и гепатита С [28], однако однозначная их связь пока не выявлена. В мета-анализе 22 исследований, включавших 1385 пациентов, спонтанная ремиссия ХСК чаще возникала у пациентов с отрицательным результатом на H. pylori по сравнению с положительным (отношение рисков 0,39; 95% ДИ 0,19-0,81) [29]. Среди пациентов с H. pylori-позитивным ХСК ремиссия крапивницы была более вероятной после эрадикационной терапии, независимо от того, была ли достигнута полная элиминация возбудителя.
Продукты питания и пищевые добавки
IgE-опосредованная пищевая аллергия часто проявляется острой крапивницей при генерализованных аллергических реакциях. При этом хронические формы заболевания редко ассоциированы с аллергией на продукты питания и пищевые добавки [30]. Несмотря на это, до половины взрослых пациентов изначально связывают эпизоды крапивницы с определенными пищевыми триггерами, особенно с обильным употреблением острой или ферментированной пищи, алкоголя или добавлением новых продуктов в рацион. Ухудшение течения крапивницы в этом случае может быть связано с содержанием гистамина в употребляемых продуктах или их неспецифическим гистамин-высвобождающими действием (продукторы-гистаминолибераторы), что характерно для алкоголя и ряда специй. Как правило, в период ремиссии хронической крапивницы употребление этих продуктов не провоцирует появление симптомов болезни.
Клиническая картина
При острой крапивнице волдыри появляются внезапно и перестают возникать менее, чем через 6 недель. В большинстве случаев эта форма крапивницы остается единственным эпизодом в жизни пациента [1].
Хронические формы характеризуются ежедневными или почти ежедневными эпизодами появления волдырей в течение 6 и более недель. Для них характерно волнообразное течение без прогрессирующего ухудшения. Ремиссия наступает в течение года у 10-30%, в течение 3-х лет у 30-50%, после 5 лет у 40-70% пациентов [31]. Наличие сопутствующего ангиоотека ассоциировано с длительностью заболевания [32].
Кожные проявления
Волдыри имеют следующие признаки:
- центральный отек разных размеров, почти всегда окруженный эритемой;
- зуд, часто мучительный, усиливающийся в ночное время, иногда с ощущением жжения;
- обратимость (каждый отдельный элемент исчезает бесследно в течение 1-24 часов).
Ангионевротический отек – частный случай крапивницы, характеризуется следующими признаками:
- быстроразвивающийся отек глубоких слоев дермы, подкожной клетчатки и подслизистого слоя;
- чувство распирания и болезненности возникают чаще, чем зуд;
- возможное отсутствие эритемы;
- разрешение в срок до 72 часов.
Кожа в месте поражения бледнее окружающих тканей, плотная (при нажатии пальцем отсутствует вдавление). Ангиоотек, как правило, сопровождается чувством распирания и иногда – боли. Зуд не характерен для этого состояния, что важно для дифференциальной диагностики с обычными проявлениями крапивницы. Наиболее частые локализации: область век, губ, щек, мошонка, крайняя плоть – т. е. области с хорошо растяжимыми тканями и рыхлой жировой клетчаткой. Реже ангиоотек поражает конечности, живот, слизистые оболочки полости рта, языка, гортани. Клиническая симптоматика обусловлена локализацией поражения [1]:
- слизистая оболочка носа – чихание и затруднение дыхания;
- губы и язык – резкое асимметричное увеличение их размеров, нарушение речи;
- гортань – осиплость голоса, вплоть до афонии (отек голосовых связок), затруднение дыхания.
Системные проявления
У небольшой части пациентов с хронической крапивницей встречаются системные симптомы:
- головная боль,
- усталость,
- артралгии и опухание суставов,
- одышка,
- нарушение функции желудочно-кишечного тракта,
- учащенное сердцебиение [33].
У пациентов с крапивницей или ангионевротическим отеком, сопровождающимися лихорадкой или объективными признаками воспаления суставов, исключают уртикарный васкулит.

Диагностика
Сбор анамнеза и физикальное обследование
При сборе анамнеза оценивают характер (вид, размер, длительность сохранения элемента, наличие зуда и ощущения распирания) и локализацию высыпаний и ангиоотеков, определяют возможные причины, с которыми пациент связывает возникновение проявлений заболевания. К возможным причинам относится прием нестероидных противовоспалительных препаратов (НПВП), а также перенесенные острые заболевания, операции или недавние обострения хронических патологий, пребывание в регионах с высоким риском заражения инфекционными или паразитарными агентами, употребление определенных продуктов питания или изменения в рационе.
Особое значение имеет непосредственное выявление врачом на приеме характерных кожных элементов [1].
Лабораторные методы диагностики
В случае острой крапивницы при указании на провоцирующий фактор в анамнезе показано проведение дообследования. При хронической крапивнице проведение обследования для выявления конкретной причины заболевания проводится всем пациентам [1].
- Общий клинический анализ крови – проводится для исключения или подтверждения наличия воспалительного процесса, оценки уровня эозинофилов и базофилов.
- Уровень С-реактивного белка (СРБ) – используется у всех пациентов с хронической и, по показаниям, острой крапивницей для исключения системного воспалительного процесса. Повышение показателя характерно для ХСК, при которой происходит массивная активация тучных клеток. Уровень СРБ коррелирует с активностью и длительностью заболевания, а также с плохим ответом на антигистаминные препараты.
- Определение уровня IgE в крови показано пациентам с хроническими и острыми формами заболевания при повторных эпизодах для уточнения патогенеза крапивницы [2].
- Определение уровня IgG к тиреопероксидазе рекомендовано пациентам с хронической крапивницей для выявления хронического аутоиммунного тиреоидита как потенциального этиологического фактора.
- Биохимический анализ крови – исследование ферментов печени и билирубина для исключения инфекционной и гастроэнтерологической патологии.
- Выявление сопутствующих хронических инфекций, в том числе инфекции Helicobacter pylori.
- Анализ на антинуклеарные антитела к Sm-антигену проводится при подозрении на системный аутоиммунный процесс как возможную причину высыпаний.
- Определение уровня и функциональной активности ингибитора С1-эстеразы рекомендовано пациентам с хронической крапивницей и ангиоотеками для дифференциальной диагностики с НАО.
- Оценка уровня С3, С4, С1q компонентов комплемента используется для дифференциальной диагностики с уртикарным васкулитом [34].
Инструментальные методы диагностики
- КТАС применяется для выявления признаков присутствия аутоантител IgG к высокоаффинному IgE-рецептору (FcϵRI) или непосредственно IgE.
- Биопсия кожи проводится при подозрении на уртикарный васкулит.
- Провокационные тесты выполняют при подозрении на определенный вариант индуцированной крапивницы. За 48 ч до проведения теста отменяют антигистаминные препараты системного действия. Выделяют разновидности провокационных тестов: холодовой, тепловой, дермографический тесты, а также тесты с давлением, с ультрафиолетовым излучением и видимым светом, с водой, с умеренной физической нагрузкой.
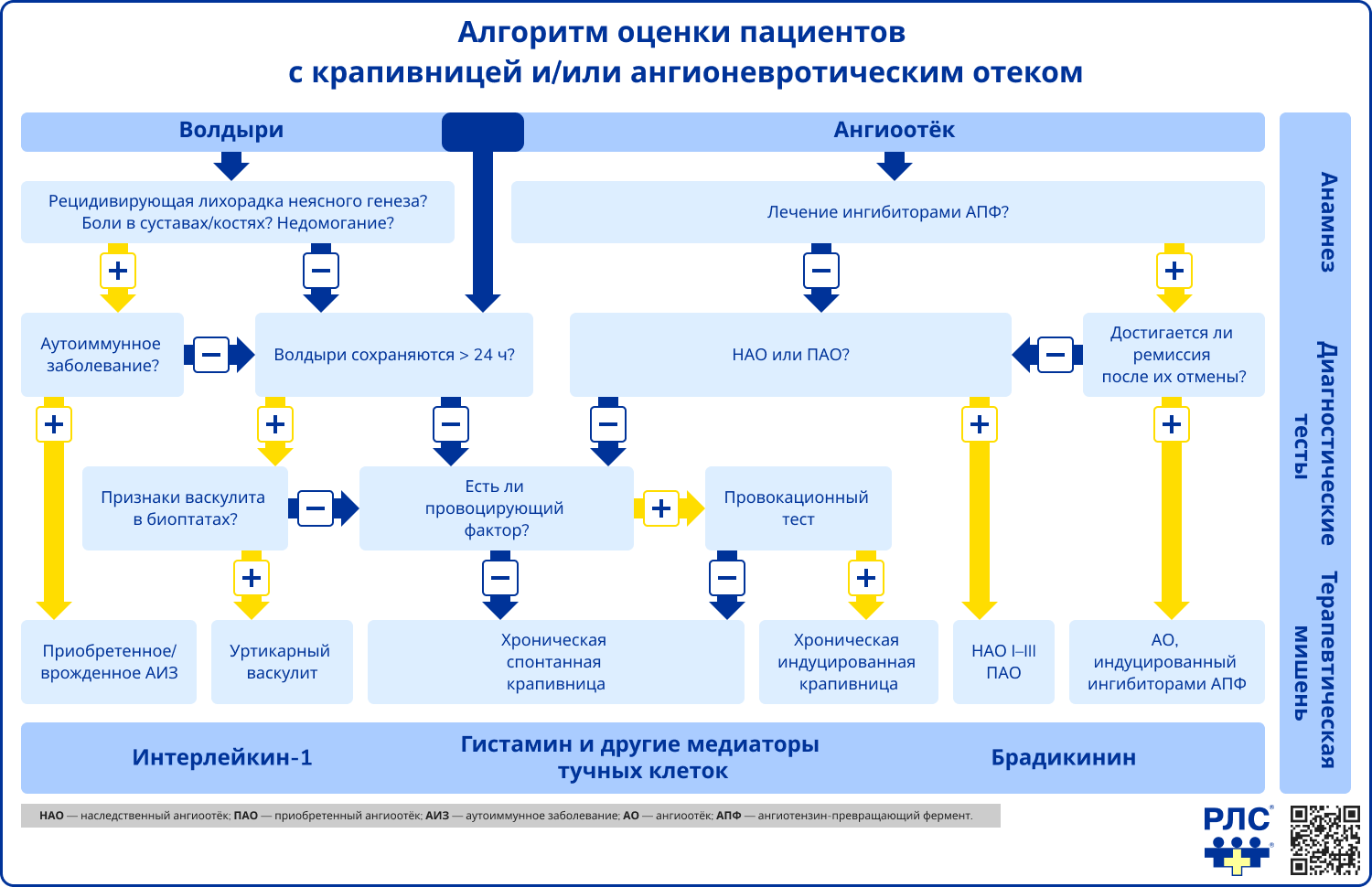
Источник: Zuberbier T., Aberer W., Asero R. The EAACI/GA²LEN/EDF/WAO guideline for the definition, classification, diagnosis and management of urticaria // Allergy – 2018. – Т. 73 – № 7 – С. 1393-1414.
Лечение
Основные принципы терапии крапивницы:
- устранение действия провоцирующих факторов,
- индукция толерантности к их воздействию в дальнейшем,
- симптоматическая терапия, направленная на снижение дегрануляции тучных клеток и устранение эффектов их медиаторов [1].
Элиминационные мероприятия
- Отмена лекарственных средств, провоцирующих появление высыпаний (например, НПВП, ингибиторы ангиотензин-превращающего фермента);
- Избегание провоцирующих симптомы условий (переохлаждение, перегревание, употребление горячей пищи и напитков, чрезмерная физическая нагрузка, нахождение на открытом солнце и т.д.);
- Лечение воспалительных и инфекционных процессов, в т.ч. эрадикация H. pylori;
- Избегание этиологически значимых продуктов в случае доказанной пищевой аллергии;
- Пациентам с ежедневными или почти ежедневными симптомами назначают «гипоаллергенную» диету, исключающую потребление продуктов с высоким содержанием гистамина (томаты, шпинат, рыба, морепродукты) и продуктов-гистаминолибераторов (клубника, шоколад, яичный белок, цитрусовые). Новый продукт можно вводить каждые 3 дня при наступлении ремиссии или клиническом улучшении течения заболевания. Половина больных хронической крапивницей через 6 месяцев возвращается к обычному питанию без возобновления симптомов заболевания.
Индукция толерантности
Индукция толерантности заключается в постоянном дозированном воздействии известного триггера и несет пользу только при некоторых типах индуцированной крапивницы (холодовой, холинэргической, солнечной). Метод не применяется рутинно из-за низкой приверженности и необходимости постоянного воздействия часто неприятного для пациента триггера (например, холода) для достижения стойкого результата [35, 36].
Симптоматическая терапия
Терапия острой крапивницы и ангиоотека
- Антигистаминные средства системного действия (неседативные, второго поколения);
- Системные глюкокортикоиды – применяются минимальным необходимым курсом для купирования острых проявлений при отсутствии эффекта от антигистаминных препаратов.
Терапия хронической крапивницы
- Антигистаминные средства системного действия (неседативные, второго поколения) – необходим длительный регулярный прием. В случае неполного эффекта этой группы препаратов дозу повышают от двукратной до четырехкратной, причем рекомендовано увеличение дозы одного антигистаминного средства, а не использование комбинации разных препаратов.
- Омализумаб – назначается пациентам с ХСК от 12 лет и старше, не получившим эффекта от антигистаминных препаратов.
- Циклоспорин – препарат третьей линии, использующийся у лиц, не ответивших на терапию антигистаминными препаратами и омализумабом. Он применяется в комбинации с антигистаминными средствами.
- Системные глюкокортикоиды – применяются для купирования тяжелых обострений максимально коротким курсом, как и для острых форм заболевания.
Список литературы
- Российская ассоциация аллергологов и клинических иммунологов (РААКИ), Общероссийская общественная организация "Российское общество дерматовенерологов и косметологов", Союз педиатров России. Клинические рекомендации "Крапивница". 2023.
- Zuberbier T. et al. The EAACI/GA²LEN/EDF/WAO guideline for the definition, classification, diagnosis and management of urticaria //Allergy. – 2018. – Т. 73. – №. 7. – С. 1393-1414.
- Confino-Cohen R. et al. Chronic urticaria and autoimmunity: associations found in a large population study //Journal of allergy and clinical immunology. – 2012. – Т. 129. – №. 5. – С. 1307-1313.
- Leznoff A., Sussman G. L. Syndrome of idiopathic chronic urticaria and angioedema with thyroid autoimmunity: a study of 90 patients //Journal of Allergy and Clinical Immunology. – 1989. – Т. 84. – №. 1. – С. 66-71.
- Grattan C. E. H. et al. A serological mediator in chronic idiopathic urticaria—a clinical, immunological and histological evaluation //British Journal of Dermatology. – 1986. – Т. 114. – №. 5. – С. 583-590.
- Eckman J. A., Hamilton R. G., Saini S. S. Independent evaluation of a commercial test for autoimmune urticaria in normal and chronic urticaria subjects //Journal of Investigative Dermatology. – 2009. – Т. 129. – №. 6. – С. 1584-1586.
- Eckman J. A. et al. Basophil phenotypes in chronic idiopathic urticaria in relation to disease activity and autoantibodies //Journal of investigative dermatology. – 2008. – Т. 128. – №. 8. – С. 1956-1963.
- Lapolla W., Desai N., English III J. C. Clinical utility of testing for autoimmunity in chronic idiopathic urticaria //Journal of the American Academy of Dermatology. – 2012. – Т. 66. – №. 3. – С. e83-e88.
- Bossi F. et al. Mast cells are critically involved in serum‐mediated vascular leakage in chronic urticaria beyond high‐affinity IgE receptor stimulation //Allergy. – 2011. – Т. 66. – №. 12. – С. 1538-1545.
- Asero R. et al. Plasma of patients with chronic urticaria shows signs of thrombin generation, and its intradermal injection causes wheal-and-flare reactions much more frequently than autologous serum //Journal of allergy and clinical immunology. – 2006. – Т. 117. – №. 5. – С. 1113-1117.
- Takahagi S. et al. Coagulation/fibrinolysis and inflammation markers are associated with disease activity in patients with chronic urticaria //Allergy. – 2010. – Т. 65. – №. 5. – С. 649-656.
- Vliagoftis H. Thrombin induces mast cell adhesion to fibronectin: evidence for involvement of protease-activated receptor-1 //The Journal of immunology. – 2002. – Т. 169. – №. 8. – С. 4551-4558.
- Huber-Lang M. et al. Generation of C5a in the absence of C3: a new complement activation pathway //Nature medicine. – 2006. – Т. 12. – №. 6. – С. 682-687.
- Kikuchi Y., Kaplan A. P. A role for C5a in augmenting IgG-dependent histamine release from basophils in chronic urticaria //Journal of allergy and clinical immunology. – 2002. – Т. 109. – №. 1. – С. 114-118.
- Takeda T. et al. Increase of coagulation potential in chronic spontaneous urticaria //Allergy. – 2011. – Т. 66. – №. 3. – С. 428-433.
- Cugno M. et al. Activation of blood coagulation in chronic urticaria: pathophysiological and clinical implications //Internal and emergency medicine. – 2010. – Т. 5. – С. 97-101.
- Mahesh P. A. et al. Effect of warfarin on chronic idiopathic urticaria //Indian Journal of Dermatology, Venereology and Leprology. – 2009. – Т. 75. – С. 187.
- Jacques P. et al. Chronic idiopathic urticaria: profiles of skin mast cell histamine release during active disease and remission //Journal of allergy and clinical immunology. – 1992. – Т. 89. – №. 6. – С. 1139-1143.
- Fujisawa D. et al. Expression of Mas-related gene X2 on mast cells is upregulated in the skin of patients with severe chronic urticaria //Journal of allergy and clinical immunology. – 2014. – Т. 134. – №. 3. – С. 622-633. e9.
- Huang A. H., Chichester K. L., Saini S. S. Association of basophil parameters with disease severity and duration in chronic spontaneous urticaria (CSU) //The journal of allergy and clinical immunology. In practice. – 2020. – Т. 8. – №. 2. – С. 793.
- Kern F. et al. Defective histamine release in chronic urticaria //The Journal of clinical investigation. – 1976. – Т. 57. – №. 5. – С. 1369-1377.
- Cohen R. W., Rosenstreich D. L. Discrimination between urticaria-prone and other allergic patients by intradermal skin testing with codeine //Journal of allergy and clinical immunology. – 1986. – Т. 77. – №. 6. – С. 802-807.
- Rauber M. M. et al. Functional and phenotypic analysis of basophils allows determining distinct subtypes in patients with chronic urticaria //Allergy. – 2017. – Т. 72. – №. 12. – С. 1904-1911.
- Bansal C. J., Bansal A. S. Stress, pseudoallergens, autoimmunity, infection and inflammation in chronic spontaneous urticaria //Allergy, Asthma & Clinical Immunology. – 2019. – Т. 15. – С. 1-11.
- Ventura M. T. et al. Anisakis simplex hypersensitivity is associated with chronic urticaria in endemic areas //International Archives of Allergy and Immunology. – 2013. – Т. 160. – №. 3. – С. 297-300.
- Başkan E. B. et al. Lack of correlation between Helicobacter pylori infection and autologous serum skin test in chronic idiopathic urticaria //International journal of dermatology. – 2005. – Т. 44. – №. 12. – С. 993-995.
- Wedi B., Raap U., Kapp A. Chronic urticaria and infections //Current opinion in allergy and clinical immunology. – 2004. – Т. 4. – №. 5. – С. 387-396.
- Daoud M. S. et al. Chronic hepatitis C and skin diseases: a review //Mayo Clinic Proceedings. – Elsevier, 1995. – Т. 70. – №. 6. – С. 559-564.
- Kim H. J. et al. Systematic review and meta‐analysis: Effect of Helicobacter pylori eradication on chronic spontaneous urticaria //Helicobacter. – 2019. – Т. 24. – №. 6. – С. e12661.
- Chung B. Y. et al. Food allergy in Korean patients with chronic urticaria //Annals of Dermatology. – 2016. – Т. 28. – №. 5. – С. 562.
- Caffarelli C. et al. Management of chronic urticaria in children: a clinical guideline //Italian journal of pediatrics. – 2019. – Т. 45. – С. 1-25.
- Toubi E. et al. Clinical and laboratory parameters in predicting chronic urticaria duration: a prospective study of 139 patients //Allergy. – 2004. – Т. 59. – №. 8. – С. 869-873.
- Doong J. C. et al. Chronic idiopathic urticaria: systemic complaints and their relationship with disease and immune measures //The Journal of Allergy and Clinical Immunology: In Practice. – 2017. – Т. 5. – №. 5. – С. 1314-1318.
- Metz M. et al. The diagnostic workup in chronic spontaneous urticaria—what to test and why //The Journal of Allergy and Clinical Immunology: In Practice. – 2021. – Т. 9. – №. 6. – С. 2274-2283.
- Beissert S., Ständer H., Schwarz T. UVA rush hardening for the treatment of solar urticaria //Journal of the American Academy of Dermatology. – 2000. – Т. 42. – №. 6. – С. 1030-1032.
- Kring Tannert L. et al. Cold urticaria patients exhibit normal skin levels of functional mast cells and histamine after tolerance induction //Dermatology. – 2012. – Т. 224. – №. 2. – С. 101-105.
Автор статьи
Статьи по теме Иммунология
- Аллергический ринит
- Пищевая аллергия
- Гиперчувствительный пневмонит
- Наследственный ангиоотек
- Атопический дерматит
- Анафилаксия
- Мастоцитоз
- Узловатая почесуха
- Бронхиальная астма
- Системная красная волчанка
- Эозинофильный эзофагит
Болезни в статье:
- D84.1 Дефект в системе комплемента
- J45.1 Неаллергическая астма
- J30 Вазомоторный и аллергический ринит
- M32 Системная красная волчанка
- M33 Дерматополимиозит
- B98.0 Helicobacter pylori [H. рylori] в качестве причины болезней, классифицированных в других рубриках
- B15 Острый гепатит A
- B18.2 Хронический вирусный гепатит C
- L27.2 Дерматит, вызванный съеденной пищей
- E06.3 Аутоиммунный тиреоидит
Фармгруппы в статье:
- H1-антигистаминные средства
- Ненаркотические анальгетики, включая нестероидные и другие противовоспалительные средства
- Ингибиторы АПФ
- Глюкокортикостероиды
Оцените статью:
- Инсектная крапивница
- Хроническая крапивница
- Идиопатическая хроническая крапивница
- Крапивница новорожденного
Что такое аллергия и как с ней бороться?
По статистике, 20% людей в мире подвержены аллергическим заболеваниям. К развитию аллергии приводит комплекс генетических, местных факторов и факторов внешней среды.
Опубликовано на сайте: 31.05.23 | Обновлено на сайте: 19.06.23
Полужирным шрифтом выделены лекарства, входящие в справочники текущего года. Рядом с названием препарата может быть указан ежегодный уровень индекса информационного спроса (показатель, который отражает степень интереса потребителей к информации о лекарстве).
крапивница
Детский возраст до 12 лет у пациентов с ХИК, крапивница, крапивнице, рецидивирующая крапивница, крапивница спровоцированная приемом ацетилсалициловой кислоты, крапивница, провоцируемая применением оцетилсалициловой кислоты или другими НПВП, обострения крапивницы спровоцированы применением ацетилсалициловой кислоты или других НПВП, хронической крапивницей, крапивница спровоцированная приемом нестероидных противовоспалительных средств, хроническая крапивница, крапивницы, крапивница, спровоцированная приемом ацетилсалициловой кислоты, крапивницей, появление крапивницы при применении препаратов с аналогичным действием, крапивница, которая усиливается при приеме ацетилсалициловой кислоты и других НПВП, появление крапивницы в случаях применения препаратов с аналогичным действием, крапивница, которая возникает при приеме ацетилсалициловой кислоты и других НПВП, крапивница спровоцированная приемом салицилатов,


 (1).png)

