M10 Подагра, МКБ-10
- M10.0 Идиопатическая подагра
- M10.1 Свинцовая подагра
- M10.2 Лекарственная подагра
- M10.3 Подагра, обусловленная нарушением почечной функции
- M10.4 Другая вторичная подагра
- M10.9 Подагра неуточненная
Отредактировано: 15.05.2026
Подагра
Определение и классификация
Подагра — это хроническое системное заболевание, обусловленное отложением кристаллов моноурата натрия в тканях на фоне стойкой гиперурикемии с последующей активацией врожденного иммунитета и развитием рецидивирующего воспалительного артрита [1, 2].
Классификация подагры носит в первую очередь клинико-патогенетический характер и отражает эволюцию заболевания во времени [2].
- Бессимптомная гиперурикемия — повышение уровня мочевой кислоты без клинических проявлений подагры.
- Острый подагрический артрит — острое воспаление, чаще моноартрит, с типичной локализацией (первый плюснефаланговый сустав). Характеризуется внезапным началом и выраженным болевым синдромом. Может разрешаться самостоятельно без лечения, однако нередко рецидивирует.
- Межприступный период — промежуток между приступами, когда симптомы отсутствуют, при этом заболевание продолжает прогрессировать.
- Хроническая тофусная подагра развивается при длительном течении заболевания и характеризуется хроническим артритом, формированием тофусов (скоплений кристаллов уратов), структурным и функциональным повреждением суставов.
По этиологии выделяют первичную и вторичную подагру. Первичная подагра обусловлена генетически детерминированными нарушениями обмена пуринов или экскреции уратов. Вторичная подагра развивается на фоне других состояний, таких как хроническая болезнь почек, миелопролиферативные заболевания, прием лекарств (например, диуретиков).
Этиология и патогенез
Подагра развивается в результате нарушения обмена пуринов, приводящего к гиперурикемии — ключевому, но не единственному фактору развития заболевания. Повышение уровня мочевой кислоты чаще всего обусловлено снижением ее выведения почками, что во многом связано с генетически детерминированными особенностями транспорта уратов. Реже причиной является избыточная продукция мочевой кислоты либо сочетание этих механизмов [1–3].
При этом важно подчеркнуть, что гиперурикемия сама по себе не означает наличие подагры: у значительной части пациентов она не приводит к клиническим проявлениям.
Формирование заболевания определяется взаимодействием метаболических и внешних факторов. К немодифицируемым относят мужской пол, возраст и генетическую предрасположенность, включая вариации генов, регулирующих почечную и кишечную экскрецию уратов. Среди модифицируемых факторов наибольшее значение имеют ожирение, употребление алкоголя (особенно пива и крепких напитков), диета с высоким содержанием пуринов и фруктозы, артериальная гипертензия, хроническая болезнь почек и применение ряда лекарственных препаратов, прежде всего диуретиков. При этом роль питания, хотя и доказана, часто переоценивается: в большинстве случаев именно нарушения экскреции уратов определяют уровень мочевой кислоты.
Патогенез подагры представляет собой последовательный процесс, в котором метаболические нарушения приводят к развитию иммуновоспалительного процесса [1–3]. При превышении порога растворимости моноурата натрия (примерно 6,8 мг/дл) создаются условия для образования кристаллов моноурата натрия. Однако сам факт гиперурикемии недостаточен: важную роль играют локальные факторы, такие как температура тканей (снижение растворимости уратов в периферических суставах), особенности внеклеточного матрикса и механические нагрузки. Эти условия способствуют кристаллизации и отложению уратов в суставах и мягких тканях.
Ключевым этапом является не столько образование кристаллов, сколько иммунный ответ на них. Кристаллы моноурата натрия фагоцитируются клетками врожденного иммунитета, прежде всего макрофагами, что приводит к активации инфламмасомы NLRP3 и высвобождению интерлейкина-1β — центрального медиатора воспаления при подагре. В дальнейшем развивается каскад воспалительных реакций с участием нейтрофилов, провоспалительных цитокинов и медиаторов, что клинически проявляется острым артритом с выраженной болью, отеком и гиперемией.
Характерной особенностью подагры является способность воспаления к спонтанному разрешению. Даже без лечения острый приступ может регрессировать, что связывают с механизмами подавления воспалительной реакции, изменением свойств кристаллов (в том числе из-за адсорбции белков на поверхности кристаллов) и устранением клеточных медиаторов воспаления. Однако при сохранении гиперурикемии происходит повторное образование и накопление кристаллов, что ведет к рецидивам, формированию тофусов и развитию хронического воспалительного процесса с прогрессирующим повреждением суставов.
Клиническая картина
Клинические проявления подагры характеризуются стадийностью и вариабельностью, отражающими накопление кристаллов моноурата натрия и эволюцию воспалительного ответа.
Острый подагрический артрит
Классическим проявлением заболевания является острый приступ артрита, который развивается внезапно, чаще в ночное время или ранние утренние часы [1–2]. Для приступа характерны следующие проявления:
- интенсивная, быстро нарастающая боль, достигающая максимума в течение нескольких часов
- отек и гиперемия сустава,
- локальное повышение температуры,
- выраженная болезненность при минимальном прикосновении [1].
Типичной локализацией поражения является первый плюснефаланговый сустав, однако могут поражаться и другие суставы: голеностопные, коленные, реже — мелкие суставы кистей [1–2]. В дебюте заболевание чаще проявляется моноартритом, но по мере прогрессирования возможно вовлечение нескольких суставов.
Общее состояние в период приступа может нарушаться: возможны субфебрильная температура, недомогание, лабораторные признаки системного воспаления (лейкоцитоз, повышение СОЭ и С-реактивного белка). Важно, что клиническая картина может имитировать инфекционный артрит, что требует осторожности в диагностике [4].
Максимальная интенсивность клинических проявлений обычно достигается в течение 12–24 часов [2]. Без лечения приступ, как правило, разрешается в течение нескольких дней или недель [1]. Однако с течением времени атаки становятся более частыми и продолжительными.
Межприступный период
После купирования острого приступа наступает бессимптомный период, в течение которого клинические проявления отсутствуют [1]. При этом патологический процесс не прекращается: кристаллы продолжают накапливаться в тканях, поддерживая субклиническое воспаление [2]. Длительность межприступного периода может составлять от нескольких месяцев до нескольких лет, однако со временем интервалы между приступами обычно сокращаются [1–2].
Хроническая тофусная подагра
При длительном течении формируется хроническая подагра. Она проявляется стойким или часто рецидивирующим артритом, вовлечением нескольких суставов и постепенным развитием структурных изменений [1–2].
Характерным признаком этой стадии является образование тофусов — плотных узловых отложений кристаллов моноурата натрия в мягких тканях. Они чаще локализуются в области ушных раковин, локтевых отростков, ахиллова сухожилия и периартикулярных тканей, могут быть безболезненными, но при повреждении кожи вскрываться с выделением белесоватого содержимого.
Подагра имеет системный характер и может сопровождаться поражением почек, включая уратную нефропатию и нефролитиаз [1]. Заболевание также часто ассоциируется с артериальной гипертензией, ожирением, сердечно-сосудистыми заболеваниями, сахарным диабетом, дислипидемией и хронической болезнью почек [2]. Эти состояния осложняют ведение подагры и способствуют преждевременной смертности [3].
В ряде случаев клиническая картина отличается от классической, что особенно характерно для пожилых, женщин или пациентов с сопутствующими заболеваниями. У них подагра может протекать атипично, с полиартритом, менее выраженной гиперемией и более постепенным началом.
Диагностика
Диагностика подагры основывается на сочетании клинической картины, лабораторных данных и инструментальных методов, однако основным диагностическим критерием является выявление кристаллов моноурата натрия (МУН).
Принципы диагностики
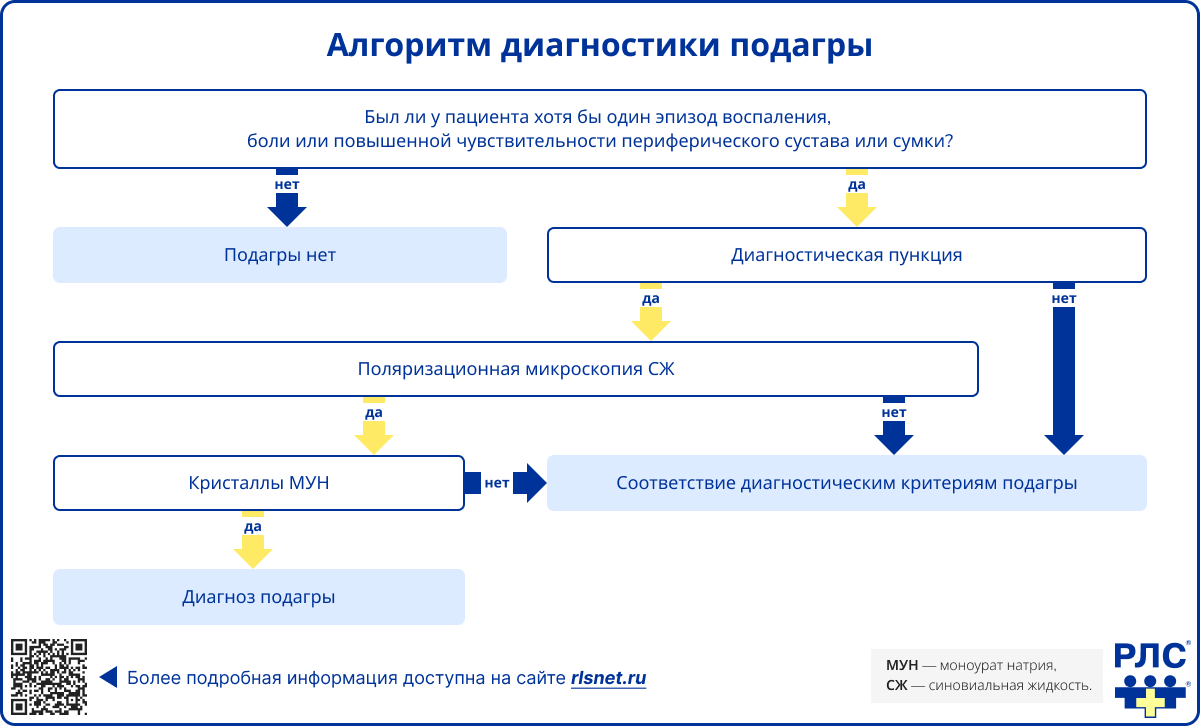
«Золотым стандартом» диагностики подагры является выявление кристаллов моноурата натрия в синовиальной жидкости или содержимом тофусов с помощью поляризационной микроскопии [1–2, 4]. Кристаллы имеют характерные признаки: игольчатую форму и отрицательное двойное лучепреломление [2].
Даже при типичной клинической картине, особенно при первом эпизоде артрита, по возможности рекомендуется проведение артроцентеза для исключения септического артрита — потенциально жизнеугрожающего состояния, способного имитировать подагру, но требующего иной тактики лечения.
В клинической практике диагноз нередко устанавливается на основании типичной клинической картины, особенно при невозможности выполнения пункции сустава. Наиболее значимые признаки включают:
- острый моноартрит с быстрым развитием симптомов,
- поражение первого плюснефалангового сустава,
- рецидивирующее течение,
- быстрый и выраженный эффект противовоспалительной терапии [1–2].
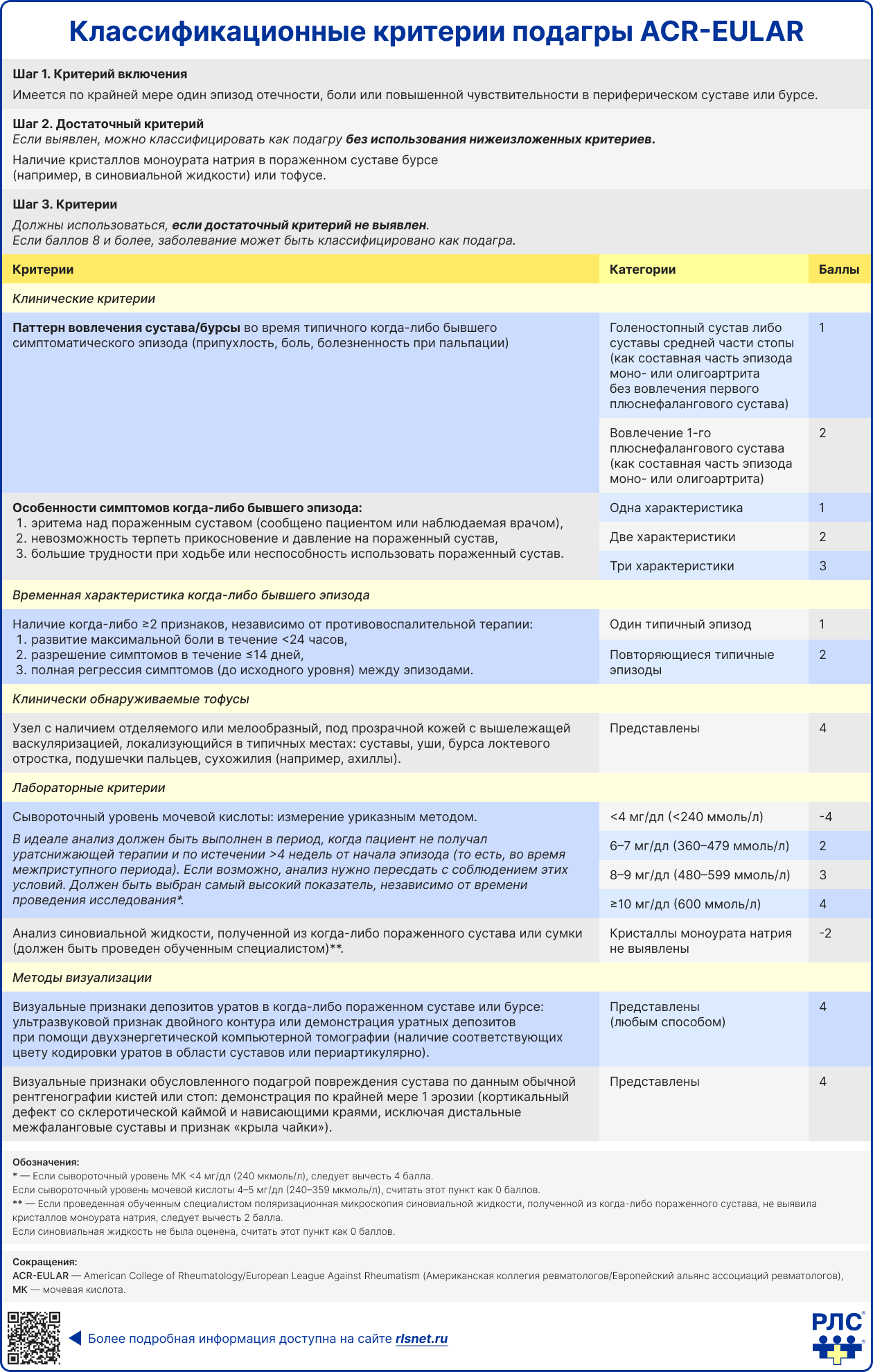
Для стандартизации используются классификационные критерии (ACR/EULAR), учитывающие клинические, лабораторные и инструментальные данные [2, 4].
Лабораторные методы
Определение уровня мочевой кислоты в сыворотке крови имеет вспомогательное диагностическое значение: гиперурикемия повышает вероятность подагры, однако сама по себе не является диагностическим критерием [1–2]. Во время острого приступа уровень мочевой кислоты в сыворотке может оставаться нормальным из-за усиления почечной экскреции уратов в острую фазу воспаления, поэтому повторное исследование рекомендуется через 2–4 недели после купирования приступа. Кроме того, гиперурикемия встречается более чем у 20% мужчин и 4% женщин в общей популяции и сама по себе не позволяет установить диагноз подагры при отсутствии клинических проявлений [2, 5].
Показатели воспаления (СОЭ, С-реактивный белок, количество лейкоцитов) могут повышаться в острую фазу заболевания, однако не обладают диагностической специфичностью [1].
Инструментальная диагностика
Инструментальные методы используются как дополнение к клинической и лабораторной для подтверждения диагноза и оценки структурных изменений, особенно при невозможности выполнения пункции сустава.
Ультразвуковое исследование может выявлять характерные признаки отложения кристаллов, такие как симптом «двойного контура» (признак отложения уратов на поверхности хряща), внутрисуставные и внутрибурсальные тофусы, а также симптом «снежной бури» [1–2]. Двухэнергетическая компьютерная томография (ДЭКТ) позволяет более специфично визуализировать отложения уратов и применяется в диагностически сложных случаях, поскольку имеет более высокую чувствительность и специфичность по сравнению с УЗИ [2]. При этом важно отметить, что оба метода имеют ограниченную чувствительность при ранней подагре, а также требуют высокого уровня профессиональной подготовки специалиста. Поэтому отсутствие отложений кристаллов МУН при УЗИ или ДЭКТ не исключает подагру, особенно на ранних стадиях заболевания.
Рентгенография информативна преимущественно на поздних стадиях, когда формируются типичные эрозии с нависающими краями (симптом пробойника) [1].
Дифференциальная диагностика
Подагру необходимо дифференцировать от:
- септического артрита,
- псевдоподагры (кальций-пирофосфатная артропатия),
- ревматоидного артрита,
- остеоартрита с воспалительным компонентом [1–2].
Лечение
Лечение подагры строится на двух взаимодополняющих направлениях: купирование острого воспаления и контроль гиперурикемии [1].
Купирование острого подагрического приступа
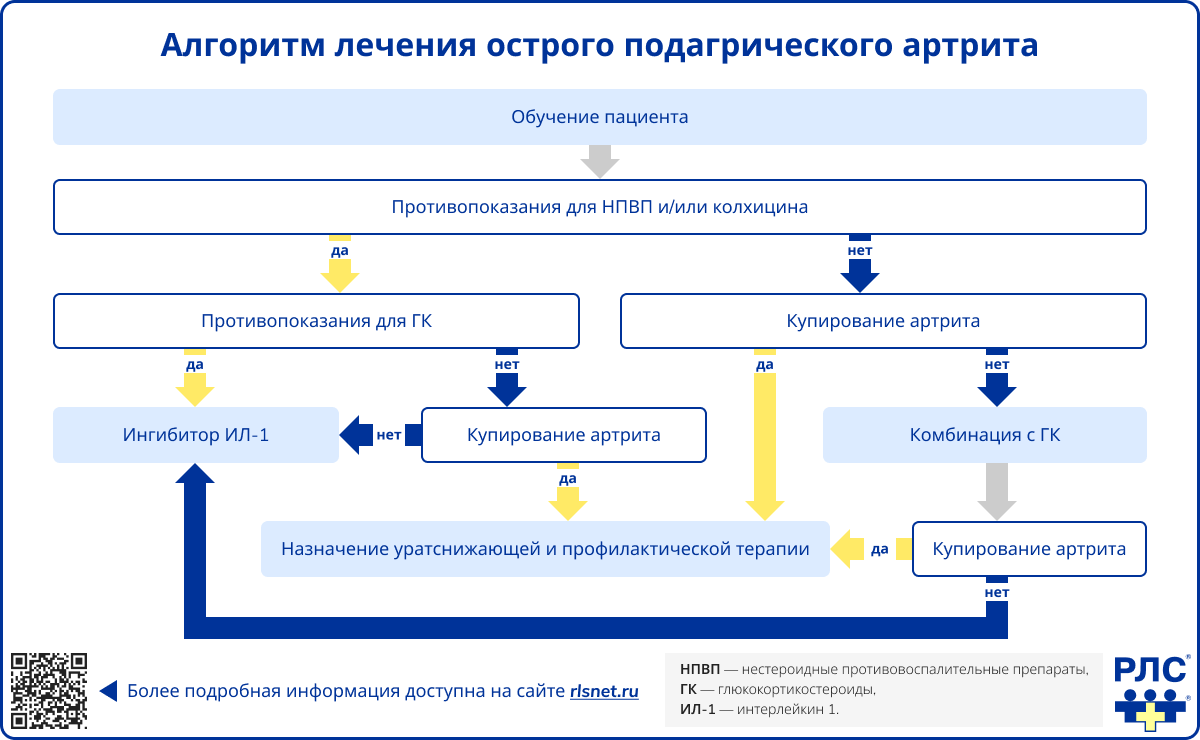
Терапия острого приступа должна быть начата как можно раньше, желательно в первые часы с момента появления симптомов, поскольку именно раннее начало лечения во многом определяет скорость регресса воспаления и выраженность анальгетического эффекта [1]. Пациенты должны быть заранее проинструктированы относительно самостоятельного начала терапии при развитии типичного приступа.
Препаратами первой линии для купирования острого подагрического артрита являются:
- нестероидные противовоспалительные препараты (НПВП),
- колхицин,
- глюкокортикостероиды (ГК) [1].
Выбор конкретного средства определяется клинической ситуацией, количеством пораженных суставов, а также наличием сопутствующих заболеваний, прежде всего хронической болезни почек (ХБП), сердечно-сосудистых заболеваний, сахарного диабета, язвенной болезни и активных инфекционных процессов [1].
НПВП назначаются внутрь в максимальных противовоспалительных дозах. Возможные режимы включают:
- нимесулид 100 мг 2 раза в сутки,
- эторикоксиб 120 мг в сутки,
- диклофенак 75 мг 2 раза в сутки,
- ибупрофен 800 мг 3 раза в сутки,
- индометацин 50 мг 3–4 раза в сутки,
- кетопрофен 100 мг 2 раза в сутки [1].
Несмотря на доказанную эффективность, НПВП следует использовать с осторожностью после оценки сердечно-сосудистого и почечного риска. При ХБП 4–5 стадии и тяжелых сердечно-сосудистых заболеваниях предпочтение следует отдавать другим вариантам терапии [1].
Колхицин наиболее эффективен при назначении в первые 12 часов с момента начала приступа. Рекомендуемый режим:
- 1 мг в начале обострения,
- затем 0,5 мг через 1 час,
- в последующие дни — по 0,5 мг 2–3 раза в сутки в зависимости от тяжести артрита [1].
Применение низкодозового режима предпочтительно, поскольку он сопоставим по эффективности с высокодозовым, но сопровождается меньшей частотой нежелательных явлений. При развитии диареи, которая рассматривается как ранний признак токсичности, дозу колхицина необходимо уменьшить или препарат отменить [1]. Особую осторожность следует соблюдать у пациентов с почечной или печеночной недостаточностью, а также при одновременном применении ингибиторов P-гликопротеина и CYP3A4.
Глюкокортикостероиды применяются при наличии противопоказаний к НПВП или колхицину, а также при определенных клинических вариантах приступа.
- Системные ГК назначаются в дозе 30–35 мг/сут в пересчете на преднизолон на 3–5 дней с последующим постепенным снижением дозы до полной отмены в течение 10–14 дней [1].
- При моноартрите крупного сустава предпочтительны внутрисуставные инъекции ГК, если сустав доступен для данной манипуляции [1].
Применение ГК требует особой осторожности у пациентов с неконтролируемым сахарным диабетом 2 типа и выраженной артериальной гипертензией [1].
При наличии абсолютных противопоказаний к НПВП, колхицину и ГК, а также при их неэффективности, в том числе в комбинации, могут использоваться ингибиторы интерлейкина-1 — канакинумаб или анакинра. Эти препараты назначаются подкожно при отсутствии противопоказаний, прежде всего активной инфекции [1].
Уратснижающую терапию во время приступа отменять не следует. Если пациент уже получает такую терапию, ее продолжают. При наличии показаний уратснижающая терапия может быть начата и в период обострения [8].
Уратснижающая терапия (базисное лечение)
Уратснижающая терапия является основным компонентом лечения подагры, поскольку именно она направлена на устранение причины заболевания — хронической гиперурикемии и связанного с ней отложения кристаллов моноурата натрия [1, 8]. Пациент должен быть информирован, что только стойкое снижение уровня мочевой кислоты позволяет добиться растворения кристаллических депозитов, прекращения приступов и регресса тофусов.
Целью терапии является достижение и поддержание сывороточного уровня мочевой кислоты:
- <360 мкмоль/л (<6 мг/дл) — у большинства пациентов,
- <300 мкмоль/л (<5 мг/дл) — при тофусной подагре и хроническом артрите [1].
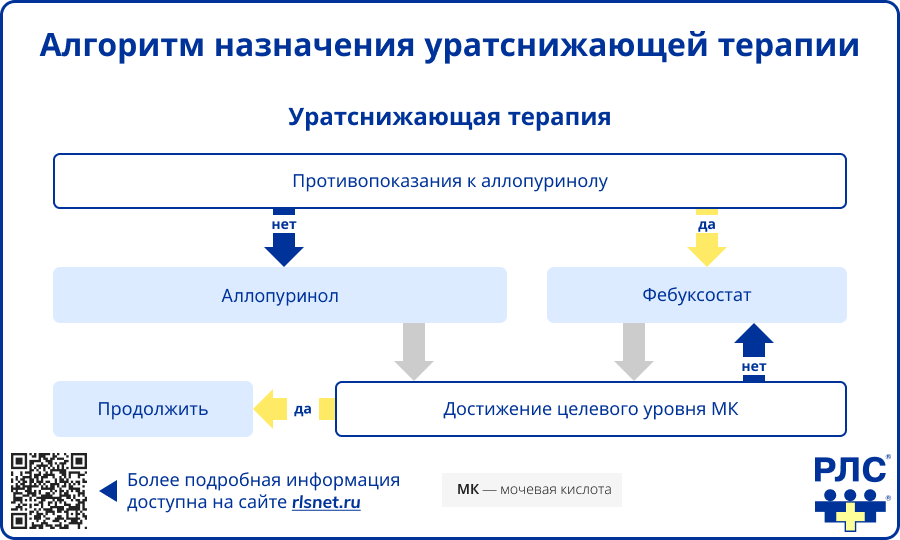
В качестве препаратов первой линии используются ингибиторы ксантиноксидазы. Препаратом выбора является аллопуринол.
- Лечение начинают с дозы 100 мг/сут с последующим титрованием по 100 мг каждые 2–4 недели до достижения целевого уровня мочевой кислоты [1].
- При необходимости доза может быть увеличена свыше 300 мг/сут, но не более 900 мг/сут [1].
Такой подход предпочтительнее длительного применения фиксированных низких доз, поскольку позволяет достигать целевого уровня мочевой кислоты у большинства пациентов.
При неэффективности аллопуринола, то есть при недостижении целевого уровня мочевой кислоты на максимально переносимой дозе, либо при его непереносимости, рекомендуется фебуксостат.
- Фебуксостат может назначаться в дозе 40 мг/сут с последующим повышением до 80–120 мг/сут при необходимости [1].
- У пациентов со сниженной функцией почек, особенно при рСКФ <60 мл/мин/1,73 м² и, в частности, <30 мл/мин/1,73 м², фебуксостат рассматривается как один из препаратов выбора, поскольку в меньшей степени зависит от почечной элиминации [1].
На этапе титрования доз аллопуринола или фебуксостата каждые 14–28 дней необходимо контролировать:
- уровень мочевой кислоты,
- уровень креатинина,
- активность АСТ и АЛТ [1].
После достижения целевого уровня мочевой кислоты уратснижающая терапия должна продолжаться длительно, как правило пожизненно. Прекращение лечения в большинстве случаев сопровождается повторным повышением уровня мочевой кислоты и рецидивами артрита [1]. Даже после достижения целевых значений необходим регулярный мониторинг уровня мочевой кислоты не реже 1 раза в 6 месяцев [1].
Дополнительными средствами, обладающими уратснижающим действием, могут быть:
- урикозурические препараты (например, пробенецид),
- уриказы при тяжелой и рефрактерной подагре (например, пеглотиказа) [1, 8].
Однако эти препараты не являются базовой терапией первой линии в рутинной практике.
Профилактика обострений
Инициация уратснижающей терапии может сопровождаться учащением приступов, особенно в первые месяцы, что связано с мобилизацией кристаллических депозитов на фоне снижения уровня мочевой кислоты [1]. По этой причине в течение первых 6 месяцев терапии всем пациентам рекомендуется медикаментозная профилактика приступов. Возможные варианты профилактики:
- колхицин 0,5–1,0 мг/сут,
- НПВП в низких дозах (например, напроксен 250 мг 2 раза в сутки, мелоксикам 7,5 мг/сут),
- низкие дозы глюкокортикостероидов (например, преднизолон 7,5 мг/сут) [1].
Колхицин рассматривается как предпочтительный препарат, поскольку противопоказания к нему встречаются реже, чем к НПВП и глюкокортикостероидам, а также имеются данные о его благоприятном влиянии на сердечно-сосудистый риск [1].
При применении НПВП для профилактики необходимо учитывать риск осложнений со стороны желудочно-кишечного тракта. У пациентов с низким риском допустимы неселективные НПВП, тогда как при повышенном риске предпочтительны селективные ингибиторы ЦОГ-2 в сочетании с ингибитором протонной помпы [1]. При высоком и очень высоком сердечно-сосудистом риске НПВП для профилактики применять не рекомендуется [1].
При длительном приеме колхицина необходимо динамическое наблюдение: не реже 1 раза в 2–3 месяца показаны клинический осмотр, общий и биохимический анализ крови, а также контроль креатинкиназы [1]. Это связано с риском редких, но тяжелых нежелательных реакций, включая миопатию, нейропатию и цитопении. При использовании низких доз глюкокортикостероидов также требуется оценка риска осложнений, включая гипергликемию, артериальную гипертензию, поражение ЖКТ и остеопороз [1].
Немедикаментозное лечение
Изменение образа жизни не заменяет медикаментозное лечение, но рассматривается как обязательный компонент комплексной терапии. Пациентам с подагрой рекомендуется:
- снижение веса при ожирении или избыточной массе тела,
- ограничение употребления алкоголя, особенно пива и крепких спиртных напитков,
- ограничение мяса красных сортов, рыбы и морепродуктов,
- ограничение фруктозосодержащих напитков,
- коррекция сопутствующих заболеваний,
- дозированная физическая нагрузка [1].
Снижение массы тела ассоциировано с уменьшением уровня мочевой кислоты и снижением частоты приступов. Ограничение алкоголя, пуриносодержащих продуктов и фруктозы также способствует уменьшению риска обострений.
Коррекция сопутствующей терапии
При наличии клинических показаний рекомендовано использовать препараты, обладающие дополнительным уратснижающим эффектом:
- лозартан — у пациентов с артериальной гипертензией,
- фенофибрат — при гипертриглицеридемии,
- ингибиторы НГЛТ-2 — у пациентов с сахарным диабетом 2 типа [1].
При этом эти препараты не рассматриваются как альтернатива базовой уратснижающей терапии, а только как полезное дополнение.
Если пациент получает петлевые или тиазидные диуретики, рекомендуется рассмотреть возможность их отмены или замены, поскольку они повышают уровень мочевой кислоты и риск подагры. Если диуретики необходимы, это не исключает возможность достижения целевого уровня мочевой кислоты, однако требует более внимательной уратснижающей терапии [1, 6].
Низкие дозы ацетилсалициловой кислоты при наличии показаний отменять не рекомендуется, поскольку их негативное влияние на мочевую кислоту считается незначительным [1].
Хирургическое лечение
Хирургическое лечение не является методом контроля подагры как метаболического заболевания, однако может потребоваться при развитии осложнений. Удаление тофусов показано при компрессии нервных структур с развитием неврологической симптоматики, в том числе при поражении позвоночника, карпального канала и других анатомических зон [1].
Эндопротезирование или артродез суставов могут рассматриваться при выраженных структурных изменениях, сопровождающихся стойким болевым синдромом и нарушением функции, если уратснижающая терапия не позволила предотвратить тяжелое поражение суставов [1].
Список литературы
- Клинические рекомендации Ассоциации ревматологов России «Идиопатическая подагра», М. 2025.
- Merriman T. «Gout: Pathophysiology» [Электронный ресурс] // UpToDate. URL: https://www.uptodate.com/contents/gout-pathophysiology (Дата обращения: 02.04.2026).
- Dalbeth N., Gosling A.L., Gaffo A., Abhishek A. Gout. Lancet. 2021 May 15;397(10287):1843-1855. doi: 10.1016/S0140-6736(21)00569-9. Epub 2021 Mar 30. Erratum in: Lancet. 2021 May 15;397(10287):1808. doi: 10.1016/S0140-6736(21)01010-2. PMID: 33798500.
- Gaffo AL. «Gout: Clinical manifestations and diagnosis» [Электронный ресурс] // UpToDate. URL: https://www.uptodate.com/contents/gout-clinical-manifestations-and-diagnosis (Дата обращения: 02.04.2026).
- Mount DB. «Asymptomatic hyperuricemia» [Электронный ресурс] // UpToDate. URL: https://www.uptodate.com/contents/asymptomatic-hyperuricemia (Дата обращения: 02.04.2026).
- Stamp LK. «Diuretic-induced hyperuricemia and gout» [Электронный ресурс] // UpToDate. URL: https://www.uptodate.com/contents/diuretic-induced-hyperuricemia-and-gout (Дата обращения: 02.04.2026).
- Neogi T. «Gout: Nonpharmacologic strategies for prevention and treatment» [Электронный ресурс] // UpToDate. URL: https://www.uptodate.com/contents/gout-nonpharmacologic-strategies-for-prevention-and-treatment (Дата обращения: 02.04.2026).
Автор статьи
Статьи по теме Ревматология
Болезни в статье:
- N18 Хроническая почечная недостаточность
- E66 Ожирение
- I10-I15 Болезни, характеризующиеся повышенным кровяным давлением
- M00-M03 Инфекционные артропатии
- N20-N23 Мочекаменная болезнь
- E10-E14 Сахарный диабет
- E78 Нарушения обмена липопротеинов и другие липидемии
- M05 Серопозитивный ревматоидный артрит
- M13.9 Артрит неуточненный
- K25 Язва желудка
- K72 Печеночная недостаточность, не классифицированная в других рубриках (в том числе печеночная кома)
- R73.9 Гипергликемия неуточненная
- M81.9 Остеопороз неуточненный
- E78.5 Гиперлипидемия неуточненная
Фармгруппы в статье:
Оцените статью:
- Обострение подагры
- Хроническая подагра
- Подагрическая атака
- Острая суставная атака при подагре
- Острый подагрический приступ
- Рецидивирующие приступы подагры
Почему подагра чаще развивается у мужчин?
Подагра считается «мужским» заболеванием — рассказываем, какие биологические и поведенческие причины стоят за этой статистикой.
Опубликовано на сайте: 12.03.26 | Обновлено на сайте: 11.03.26
Полужирным шрифтом выделены лекарства, входящие в справочники текущего года. Рядом с названием препарата может быть указан ежегодный уровень индекса информационного спроса (показатель, который отражает степень интереса потребителей к информации о лекарстве).
подагра
подагра, острый приступ подагры, пациенты с подагрическим артритом, при применении у пациентов с подагрои, подагрой, подагре, острой подагре, острая подагра, проявления подагры, подагрический артрит, гиперурикемия, проявляющаяся подагрой, подагры,




