E28.2 Синдром поликистоза яичников, МКБ-10
Отредактировано: 24.03.2026
Синдром поликистозных яичников
Определение и классификация
Синдром поликистозных яичников (СПЯ, синдром Штейна-Левенталя) – полигенное эндокринное заболевание, обусловленное как генетическими, так и эпигенетическими факторами, включающее комплекс репродуктивных, метаболических и психологических особенностей. Клинические проявления СПЯ, алгоритмы диагностики и лечения имеют различия в зависимости от возраста пациентки [1].
Критерии диагностики СПЯ названы Роттердамскими, т.к. были приняты в 2003 году в г. Роттердам (Нидерланды) на Международном симпозиуме, объединившем рабочие группы ESHRE и ASRM [2].
Диагноз СПЯ устанавливается при наличии не менее двух из трёх признаков [3]:
- Олигоановуляция;
- Гиперандрогения (клинические или лабораторные признаки);
- Поликистозная морфология яичников по данным УЗИ.
Учитывая многообразие клинических вариантов СПЯ, рекомендуется относить пациентку к одному из фенотипов, соответствующих четырём возможным комбинациям диагностических признаков [4]:
- Классический,
- Ановуляторный,
- Овуляторный,
- Неандрогенный.

Источник: National Institutes of Health: Evidence-based methodology workshop on polycystic ovary syndrome. December 3-5, 2012. Executive summary. Final report. Available at: https://prcvention.nih.gov/sitcs/defaultf£1es/2018-06/ FinaiRcport.pdf. Accessed June 24, 2019.
Этиология и патогенез
Общепринятой концепции происхождения СПЯ не разработано. Нарушения функции репродуктивной системы наблюдаются на четырёх уровнях:
- гипоталамо-гипофизарной системы,
- яичников,
- надпочечников,
- периферических инсулин-чувствительных тканей.
Невозможно на теущем этапе изученности заболевания выделить повреждение какого-либо из четырёх перечисленных уровней как основополагающее [5, 6].
Были получены убедительные данные в пользу того, что СПЯ является наследственным заболеванием. Предполагается аутосомное доминантное наследование, проявляющееся не только у женщин, но и мужчин. У мужчин, чьи близкие родственницы страдают СПЯ, чаще наблюдается повышение уровня дигидроэпиандростерон-сульфата (ДГЭАС) в крови, ранняя алопеция, инсулинорезистентность и другие метаболические нарушения, характерные для СПЯ [5, 7, 8].
Патогенез ановуляции
Нарушение ритма секреции гонадотропин-рилизинг-гормона (ГнРГ) ведёт к преобладанию выработки ЛГ над ФСГ. Окончательно не установлено, является ли дисфункция гипоталамуса первичной или вторичной по отношению к изменению баланса стероидных гормонов и нарушению отрицательной обратной связи. В пользу гипоталамического генеза СПЯ свидетельствует высокая встречаемость диэнцефальных симптомов среди пациенток [6].
Изменение секреции ГнРГ и повышение соотношения ЛГ: ФСГ приводит к нарушению созревания фолликулов яичника и подавлению овуляции. Однако это не единственный механизм: ановуляции способствуют также гиперандрогения и инсулинорезистентность.
Патогенез инсулинорезистентности
Инсулинорезистентность характерна для пациенток с СПЯ независимо от наличия ожирения. Предполагаемый механизм заключается в дефекте внутриклеточной передачи сигнала после связывания инсулина с рецептором [5, 9].
Гиперинсулинемия стимулирует рост кератиноцитов и фибробластов, что ведёт к появлению чёрного акантоза. Эти характерные изменения кожи имеют вид толстых серо-коричневых бляшек в бархатистой поверхностью, которые локализуются в области естественных складок кожи: на шее, в подмышках, в инфрамаммарных складках, в паху, на пояснице [10]. Несмотря на то, что инсулинорезистентность при СПЯ не всегда ассоциирована с ожирением, при метаболическом синдроме и избыточном весе чёрный акантоз встречается чаще [11, 12].
Инсулинорезистентность обусловливает долгосрочные осложнения СПЯ, включая сахарный диабет, артериальную гипертензию, дислипидемию и сердечно-сосудистые заболевания [5].
Патогенез гиперандрогении
Повышенные уровни ЛГ и инсулина стимулируют избыточную секрецию андрогенов тека-клетками яичника – тестостерона и андростендиона.
В волосяном фолликуле под действием 5α-редуктазы тестостерон преобразуется в дигидротестостерон, обладающий более выраженным эффектом на волосяные фолликулы пушковых волос. Пушковые волосы, фолликулы которых содержат рецепторы к андрогенам, преобразуются в терминальные волосы. Чувствительные к действию андрогенов области включают верхнюю губу, подбородок, зону роста бакенбард, грудь, белую линию нижней части живота. Напротив, терминальные волосы в андроген-независимых областях под действием избытка андрогенов преобразуются в пушковые волосы, что проявляется алопецией.
Гиперстимуляция андрогенных рецепторов сальных желёз ведёт к повышенной секреции себума. В сочетании с гиперинсулинемией, предрасполагающей к гиперкератозу, возникают условия, благоприятные для закупорки протоков сальных желёз, формирования комедонов и размножения Propionibacterium acnes. Перечисленные процессы приводят к воспалению, развитию акне, в исходе которого на коже остаются рубцы.
Помимо абсолютной гиперандрогении, для пациенток с СПЯ характерно снижение уровня глобулина, связывающего половые стероиды (ПССГ). Синтез ПССГ подавляют андрогены, инсулин, глюкокортикоиды, гестагены и гормон роста. В ряде случаев у пациенток с СПЯ общий уровень тестостерона соответствует нормативным значениям, однако недостаток синтеза ПССГ приводит к относительной гиперандрогении с соответствующими клиническими проявлениями.
Ещё одно следствие гиперандрогении – повышение риска гиперплазии и рака эндометрия. Избыток андростендиона под действием периферической ароматазы преобразуется в эстрон. Избыток эстрона приводит к двоякому эффекту. С одной стороны, влияние на гипоталамус и гипофиз по механизму отрицательной обратной связи поддерживает недостаток ФСГ и избыток ЛГ, следовательно, способствует ановуляции. С другой стороны, постоянное действие эстрона на эндометрий при отсутствии циклических колебаний уровня половых гормонов и в условиях олигоменореи приводит к избыточной пролиферации и гиперпластическим процессам.

Источник: Barbara L. Hoffman, John 0. Schorge, Lisa M. Halvorson, Cherine A. Hamid, Marlene M. Corton, Joseph I. Schaffer. Williams Gynecology, 4th edition изд. New-York: McGraw Hill Professional, 2020.
Клиническая картина
СПЯ включает следующие клинические признаки:
- нарушения менструального цикла:
- олигоменорею начиная с менархе, наступившего в срок,
- аменорею у нелечённых женщин старше 30 лет;
- бесплодие;
- гирсутизм;
- угревую сыпь;
- ожирение;
- чёрный акантоз.
Фенотипы СПЯ разнообразны и зависят от возраста пациентки. Перечисленные симптомы присутствуют не во всех случаях, однако их сочетание требует исключения СПЯ [1].
Диагностика
Физикальное обследование
При сборе анамнеза обращают внимание на наличие сахарного диабета (как 1, так и 2 типа) у пациентки, а также родственников с сахарным диабетом 2 типа.
При сборе жалоб уточняют характер менструального цикла. Нерегулярные менструации в первый год после менархе представляют из себя физиологическое явление. В дальнейшем менструальный цикл оценивается как нерегулярный, если:
- в срок более 1 года, но менее 3 лет после менархе продолжительность цикла составляет <21 или >45 дней;
- в срок более 1 года после менархе продолжительность цикла более 90 дней;
- в срок более 3 лет после менархе продолжительность цикла <24 или >38 дней, или за год происходит менее 9 циклов.
Если выявлены жалобы на нерегулярные менструации, в числе возможных причин рассматривают СПЯ.
Необходимо учитывать, что даже регулярные менструации могут сопровождаться ановуляцией [13].
При общем осмотре для выявления ожирения рассчитывают индекс массы тела (ИМТ):
ИМТ = масса тела (кг)/рост2 (м2)

Для определения типа ожирения измеряют окружность талии (ОТ). У женщин ОТ >80 см свидетельствует об абдоминальном типе ожирения, напрямую связанном с инсулинорезистентностью.
У пациенток с ожирением уточняют наличие жалоб, являющихся признаками синдрома обструктивного апноэ сна (СОАС): храп, ощущение разбитости по утрам, усталость и сонливость в течение дня. Для объективизации жалоб используют Берлинский опросник.
Выраженность гирсутизма оценивают по модифицированной шкале Ферримана-Галлвея. Оценивают по 4-балльной шкале рост волос в каждой из областей: верхняя губа, подбородок, грудь, белая линия верхней части живота, белая линия нижней части живота, плечи, бёдра, спина, ягодицы. Сумма баллов называется гирсутным числом. Гирсутизм диагностируется, если гирсутное число составляет 4-6 баллов. У представительниц Юго-Восточной Азии диагностически значимой является сумма баллов ≥3 [1, 14].
Пациентки могут рутинно прибегать к косметическим процедурам, маскирующим проявления гирсутизма. Однако для адекватной оценки гирсутного числа по шкале Ферримана-Галлвея пациентка не должна прибегать к эпиляции или депиляции в течение 4 недель и не сбривать волосы в срок не менее 5 дней до момента исследования. Поскольку гирсутизм представляет из себя проблему, влияющую на самооценку и психологическое состояние женщин, страдающих СПЯ, в ряде случаев затруднительно выполнить эти условия [13].
Для оценки алопеции рекомендуется использовать шкалы Людвига или Ольсена, в зависимости от паттерна облысения [1, 13].
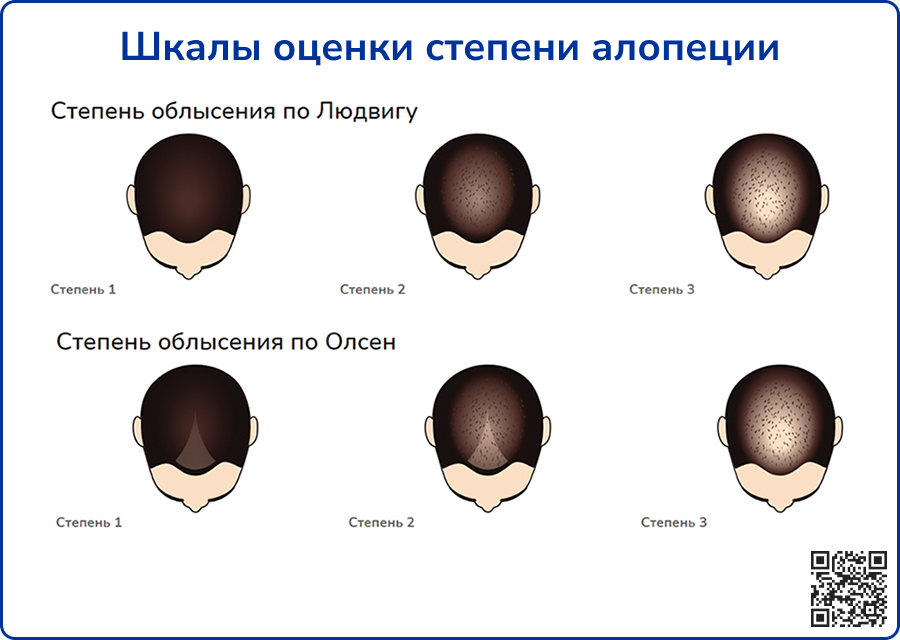
Источник: https://netvolos.ru/patsientam/stepen-oblyseniya-u-zhenschin/ от 27.10.2023.
При осмотре оценивают также наличие акне и чёрного акантоза.
Необходимо учитывать, что алопеция и акне не относятся к специфическим признакам гиперандрогении [1].
Учитывая повышенный риск артериальной гипертензии, пациенткам с диагностированным СПКЯ показано измерение артериального давления на каждом приёме [13].
Лабораторные исследования
Оценка уровня андрогенов, в зависимости от клинической ситуации, включает несколько этапов.
1. Всем пациенткам с подозрением на СПЯ рекомендуется исследование общего тестостерона и ПССГ в крови.
2. Полученные данные используют для расчёта индекса свободных андрогенов (ИСА), который характеризует уровень свободного, т. е. биологически активного, тестостерона.
ИСА = общий тестостерон (нмоль/л)/ПССГ (нмоль/л)

3. При необходимости прямого определения свободного тестостерона используют метод жидкостной хроматографии с масс-спектрометрией [13]. Не рекомендуется использовать методы, основанные на иммуноферментном и радиометрическом анализе, из-за низкой чувствительности и специфичности. Референсные значения зависят от технических особенностей лаборатории. Оценка уровня свободного тестостерона с помощью ИСА является предпочтительным методом.
4. Если у пациенток с подозрением на СПЯ не выявлено повышения общего или свободного тестостерона, измеряют уровень ДГЭАС и андростендиона в крови.
При диагностике СПЯ у подростков важно учитывать, что уровень андрогенов соответствует таковому у женщин репродуктивного возраста с 12-15 лет.
У женщин, принимающих комбинированные оральные контрацептивы (КОК), происходит подавление синтеза ПССГ и снижение гонадотропин-опосредованной выработки андрогенов. Следовательно, определение уровня андрогенов в крови не даёт достоверных данных о наличии или отсутствии их избыточного синтеза. Если оценка биохимической гиперандрогении критически необходима, рекомендовано провести исследование через 3 месяца после отмены КОК. На время отмены препарата назначается негормональная контрацепция.
Всем пациенткам с СПЯ показана оценка гликемии. Предпочтительный метод – пероральный глюкозотолерантный тест (ПГТТ) с 75 г глюкозы. При отсутствии возможности проведения этого теста рекомендовано исследование глюкозы плазмы крови натощак или гликированного гемоглобина (HbA1c). Контроль гликемии проводится пациенткам с СПЯ каждые 1-3 года, в зависимости от степени риска развития сахарного диабета. Если диагностируется сахарный диабет, лечение проводится в соответствии с текущими клиническими рекомендациями [1, 13].
Для оценки инсулинорезистентности используют индексы HOMA (Homeostasis model assessment) и Caro.
Расчёт индекса HOMA:
HOMA = уровень глюкозы натощак (ммоль/л)*уровень инсулина натощак (мЕд/л)/22,5
Нормальное значение <3,9.
Расчёт индекса Caro:
Индекс Caro = уровень глюкозы натощак (ммоль/л)/уровень инсулина натощак (мкМЕ/мл)
Нормальное значение ≥0,33 [1, 15].
Изолированное определение инсулина плазмы крови для оценки инсулинорезистентности не рекомендуется [1].
В рекомендациях ESHRE по СПЯ 2023 года оценка индексов инсулинорезистентности также не входит в перечень рутинно необходимых исследований [13].
Исследование уровня антимюллерова гормона (АМГ) не относится к обязательным для диагностики СПЯ [1].
Инструментальные исследования
Пациенткам с подозрением на СПЯ рекомендуется УЗИ органов малого таза, подсчёт фолликулов и определение объёма яичников. Предпочтительным методом у женщин, живущих половой жизнью, является трансвагинальное УЗИ. Исследование проводится в фолликулярную фазу, у женщин с олиго- или аменореей – либо независимо от фазы цикла, либо на 3-5 день менструальноподобной реакции после пробы с прогестероном.
Критерии поликистоза яичников:
- ≥20 фолликулов диаметром 2-9 мм в одном яичнике при подсчёте с помощью трансвагинального датчика с частотой сигнала 8 МГц и/или объём яичника ≥10 см3;
- при использовании датчика с меньшей частотой сигнала: объём яичника ≥10 см3 или >10 фолликулов в одном сечении одного яичника [1, 13].
Эти критерии применимы для пациенток репродуктивного возраста. У подростков в течение 8 лет после менархе не рекомендуется диагностировать СПЯ по УЗИ-критериям, т. к. поликистозная структура яичников часто встречается в этом возрасте, в т.ч. у здоровых девушек.
Если при УЗИ наблюдаются доминантный фолликул, жёлтое тело или кисты яичника, рекомендовано повторение исследования после очередной спонтанной или индуцированной менструации [1].
При первичной консультации рекомендуется оценка липидного профиля [1].
Иные исследования
Для уточнения овуляторной дисфункции у пациенток с СПЯ репродуктивного возраста возможно сочетанное применение лабораторных и инструментальных исследований:
- определение прогестерона в крови на 6-8 день после овуляции; уровень прогестерона менее 3 нг/мл свидетельствует об ановуляции, уровень менее 10 нг/мл или суммарное содержание в трёх последовательных пробах менее 30 нг/мл – о недостаточности лютеиновой фазы;
- оценка функции яичников по данным УЗИ органов малого таза на 21-22 день менструального цикла.
Пациенткам с ИМТ более 25 кг/м2 рекомендуется полисомнографическое исследование для исключения синдрома обструктивного апноэ сна.
Женщинам с СПЯ проводят скрининг на тревожно-депрессивные расстройства, т.к. последние часто встречаются у пациенток этой группы. Рекомендуется также диагностировать расстройства пищевого поведения и психологические аспекты сексуальной дисфункции [1, 13].
Лечение
В терапии СПЯ выделяют несколько направлений:
- коррекция клинических проявлений гиперандрогении,
- устранение ожирения и метаболических нарушений,
- возвращение овуляторных менструальных циклов и фертильности,
- предотвращение осложнений.
Модификация образа жизни
Для нормализации углеводного и липидного обмена, снижения риска сердечно-сосудистых заболеваний, нормализации массы тела и повышения качества жизни важна модификация образа жизни. В это понятие входят сбалансированная диета и достаточная физическая активность.
Нет доказательств преимущества определённой диеты с точки зрения эффективности снижения веса. Не рекомендуется использовать чрезмерно ограничительные и несбалансированные диеты. Благоприятным считается снижение массы тела на 5-10% за 6 месяцев. Такая скорость похудения улучшает прогноз заболевания и в то же время является оптимальной для адаптации метаболизма.
Минимальная физическая нагрузка для людей возраста 18-64 лет должна составлять:
- 150 минут в неделю физической активности средней интенсивности;
- или 75 минут в неделю физической активности высокой интенсивности;
- или эквивалентное сочетание средней и высокой нагрузки.
Желательно включение упражнений, направленных на укрепление мышц, в течение двух дней в неделю, не следующих друг за другом.
Минимальная физическая нагрузка препятствует увеличению веса и улучшает общее состояние здоровья. Для снижения веса той же возрастной категории рекомендован более интенсивный режим:
- 250 минут в неделю физической активности средней интенсивности;
- или 150 минут в неделю физической активности высокой интенсивности;
- или эквивалентное сочетание средней и высокой нагрузки.
Подросткам рекомендуется режим тренировок средней и высокой интенсивности по 60 минут в день 3 дня в неделю, с включением упражнений на укрепление мышц и костей.
Модификация образа жизни требует доверительного отношения с пациенткой, сознательного подхода женщины к собственному здоровью. Здоровый образ жизни даже при отсутствии снижения веса ассоциирован с благоприятными долгосрочными последствиями: предотвращает дальнейшее увеличение массы тела, приводит к перераспределению жировой ткани с уменьшением количества абдоминального жира.
Для повышения мотивации пациентки возможно применение психологических техник, в т.ч. когнитивно-поведенческой терапии и установки SMART-цели (Specific, Measurable, Achievable, Realistic and Timely – конкретная, измеримая, достижимая, реалистичная, ограниченная во времени цель). Общие рекомендации в ряде случаев приходится адаптировать под медицинские, психологические и социальные ограничения конкретной пациентки. Учитывая повышенную встречаемость расстройств пищевого поведения среди женщин с СПЯ, лечащему врачу приходится проявлять особый такт, обсуждая проблему снижения веса. Для повышения комфорта пациентки при контроле динамики массы тела можно использовать взвешивание вслепую (метод, при котором медицинский персонал не сообщает пациенту результат измерения, не комментирует изменения массы тела). Поддержка и участие семьи в соблюдении диеты и регулярных физических упражнениях может также оказать пользу [1, 13, 16, 17, 18].
Медикаментозная терапия
Комбинированные гормональные контрацептивы (КОК, трансдермальные пластыри, вагинальные кольца) показаны пациенткам с СПЯ, нарушениями менструального цикла и клиническими проявлениями гиперандрогении.
Механизм действия КГК:
- Ингибирование выработки ЛГ, что препятствует стимуляции синтеза андрогенов в клетках теки яичников;
- Снижение продукции надпочечниковых андрогенов за счёт подавления синтеза АКТГ;
- Эстрогенный компонент повышает синтез ПССГ, снижая, таким образом, уровень свободного тестостерона;
- Гестагенный компонент конкурентно ингибирует 5α-редуктазу.
Препараты, содержащие 35 мкг этинилэстрадиола и ципротерон, не рекомендуется назначать в первой линии терапии, т.к. их применение связано с повышенным риском тромбоэмболических осложнений. Этот побочный эффект приобретает особое значение при лечении СПЯ, который связан с повышенным риском сердечно-сосудистых заболеваний, в остальных случаях нехарактерных для женщин репродуктивного возраста.
Необходимо подбирать КГК с гестагенами, приём которых не приводит к увеличению веса.
КОК, содержащие фолаты, имеют преимущества, т. к. способны компенсировать гипергомоцистеинемию. Это состояние часто наблюдается у пациенток с СПЯ, сопряжено с повышенным риском сердечно-сосудистых заболеваний и возникает при недостатке фолиевой кислоты.
Антиандрогены назначают в дополнение к КГК, если через 6 месяцев применения не наблюдается значительного улучшения симптомов гиперандрогении:
- ципротерон – для лечения акне и гирсутизма;
- спиронолактон – для лечения акне;
- финастерид, флутамид (не зарегистрированы в России) – для лечения гирсутизма.
Метформин используют как препарат второй линии для лечения пациенток, которым противопоказаны КГК. Метформин также показан при лечении ановуляции: как для самостоятельного применения, так и в сочетании с кломифеном.
Фармакотерапия ожирения: орлистат, лираглутид, сибутрамин. Комбинация КОК и орлистата повышает эффективность снижения веса и нормализации липидного обмена. При назначении сибутрамина показана оценка сердечно-сосудистых рисков.
Летрозол – препарат первой линии для стимуляции овуляции по международным клиническим рекомендациям [13]. В России назначается off-label, после получения добровольного информированного согласия пациентки.
Кломифен используют для лечения ановуляции. Назначение кломифена рекомендовано после модификации образа жизни и исключения других причин бесплодия, помимо СПЯ. Предикторы неэффективности кломифена: повышенный ИСА, избыточный вес или ожирение, аменорея, увеличение объёма яичников.
Препараты гонадотропинов применяют в качестве второй линии терапии ановуляции. Применение гонадотропинов требует УЗИ-контроля овариального ответа.
Хирургическое лечение
Лапароскопический дриллинг яичников сопоставим по эффективности с препаратами гонадотропинов и относится ко второй линии терапии. Дриллинг – создание отверстий на поверхности яичника глубиной 0,5 мм на расстоянии не менее 1 см друг от друга. Метод был изобретён эмпирически, однако предполагается, что эффект манипуляции обусловлен снижением объёма андроген-продуцирующей ткани. Необходимо учитывать, что при воздействии на кору яичника неизбежно снижается овариальный резерв. Рекомендуется при лапароскопическом дриллинге создавать 4 отверстия – количество, достаточное для возникновения овуляции. При большем количестве отверстий высок риск развития преждевременной недостаточности яичника. Предпочтительные методы дриллинга – монополярная коагуляция (электрокаутеризация) и лазерная вапоризация. Биполярная коагуляция (диатермокоагуляция) нежелательна, т.к. ведёт к более обширному повреждению ткани яичника [1, 19].
Бариатрическая хирургия при СПЯ рекомендована пациенткам с ИМТ ≥40 кг/м2 или с ИМТ ≥35 кг/м2 при наличии осложнений, связанных с ожирением [1]. Было показано, что коррекция ожирения с помощью бариатрической операции способствует лечению бесплодия и рождению здорового ребёнка [20, 21].
Список литературы
- Адамян Л.В., Андреева Е.Н., Абсатарова Ю.С., Григорян О.Р., Дедов И.И., Мельниченко Г.А., Сутурина Л.В., Филиппов О.С., Шереметьева Е.В., Чернуха Г.Е., Ярмолинская М.И. Клинические рекомендации “Синдром поликистозных яичников”. 2022. doi: 10.14341/probl12874
- Д.Е.Шилин. Международный диагностический консенсус (2003 г.) и современная идеология терапии. CONSILIUM-MEDICUM 06/N 9/2004.
- The Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group: Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome (PCOS). Hum Rcprod 19:41, 2004.
- National Institutes of Health: Evidence-based methodology workshop on polycystic ovary syndrome. December 3-5, 2012. Executive summary. Final report. Available at: https://prcvention.nih.gov/sitcs/defaultf£1es/2018-06/ FinaiRcport.pdf. Accessed June 24, 2019.
- Barbara L. Hoffman, John 0. Schorge, Lisa M. Halvorson, Cherine A. Hamid, Marlene M. Corton, Joseph I. Schaffer. Williams Gynecology, 4th edition изд. New-York: McGraw Hill Professional, 2020.
- Гинекология. Национальное руководство. Краткое издание / под ред. Г. М. Савельевой, Г. Т. Сухих, И. Б. Манухина. — М.: ГЭОТАР Медиа, 2013. — 704 с. ISBN 978-5-9704-2662-3.
- Cannarella R, Condorelli RA. Mongiol LM, et al: Does a male polycystic ovarian syndrome equivalent exist? J Endocrinol Invest 41(1):49, 2018.
- Torchen LC, Kumar A, Kalra B, et al: Increased antimiillerian hormone levels and other reproductive endocrine changes in adult male rdatives of women with polycystic ovary syndrome. Fertil Steril106(1):50, 2016.
- Dunaif A: Insulin resistance and the polycystic ovary syndrome: mechanisms and implication for pathogenesis. Endocr Rev 18:774, 1997.
- Panidis D, Sltiadopoulos S, Rousso D, et al: Association of acanthosis nigricans with insulin resistance in patients with polycystic ovary syndrome. Br J Dermatol 132:936, 1995.
- Kazemi M, Pierson RA, Lujan ME, et al: Comprehensive evaluation of type 2 diabetes and cardiovascular disease risk profiles in reproductive-age women with polycystic ovary syndrome: a large Canadian cohort. J Obstet Gynaecol Can 41(10):1453, 2019.
- Reyes-Mutioz E, Ortega-Gonzalez C, Martinez-Cruz N, et al: Association of obesity and overweight with the prevalence of insulin resistance, prediabetes and clinical-biochemical characteristics among infertile Maican women with polycystic ovary syndrome: a cross-sectional study. BMJ Open 6(7):e012107, 2016.
- Helena Teede et al. (full authorship above). International Evidence-based Guideline for the Assessment and Management of Polycystic Ovary Syndrome 2023. Monash University. https://doi.org/10.26180/24003834.v1
- Yildiz, B. O. et al. Visually scoring hirsutism. Human reproduction update, 16(1), 51-64. 2010.
- Jeanes YM, Reeves S. Metabolic consequences of obesity and insulin resistance in polycystic ovary syndrome: diagnostic and methodological challenges. Nutr Res Rev. 2017 Jun;30(1):97-105.
- Lim SS, Hutchison SK, Van Ryswyk E, Norman RJ, Teede HJ, Moran LJ. Lifestyle changes in women with polycystic ovary syndrome. Cochrane Database Syst Rev 2019; 3:CD007506.
- Oberg E, Gidlof S, Jakson I, Mitsell M, Tollet Egnell P, Hirschberg AL. Improved menstrual function in obese women with polycystic ovary syndrome after behavioural modification intervention-A randomized controlled trial. Clin Endocrinol (Oxf) 2019; 90:468-478.
- Dos Santos IK, Ashe MC, Cobucci RN, Soares GM, de Oliveira Maranhao TM, Dantas PMS. The effect of exercise as an intervention for women with polycystic ovary syndrome: A systematic review and meta-analysis. Medicine (Baltimore) 2020; 99:e19644.
- Е.Н. Андреева, Е.В. Шереметьева, А.С. Аракелян. Хирургические аспекты лечения синдрома поликистозных яичников. Проблемы репродукции 2020, Т. 26, №5, с. 65-71 https://doi.org/10.17116/repro20202605165
- Singh D, Arumalla K, Aggarwal S, Singla V, Ganie A, Malhotra N. Impact of Bariatric Surgery on Clinical, Biochemical, and Hormonal Parameters in Women with Polycystic Ovary Syndrome (PCOS). ObesSurg. 2020 Jun;30(6):2294-2300.
- Thessaloniki ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group. Consensus on infertility treatment related to polycystic ovary syndrome. Hum Reprod. 2008;23(3):462-77.
Чтобы проверить свои знания материала, пройдите квиз. Кликните на картинку, чтобы начать.
Описание проверено экспертом
Статьи по теме Акушерство и гинекология
- Аномальные маточные кровотечения
- Дисменорея
- Преэклампсия
- HELLP-синдром
- Синдром предменструального напряжения
- Аменорея и олигоменорея
- Менопауза и климактерический синдром
- Инфекции мочевыводящих путей при беременности
- Хламидийная инфекция
- Гонококковая инфекция
- Урогенитальный трихомониаз
- Синдром гиперстимуляции яичников
- Акушерская тромбоэмболия
- Врожденная дисфункция коры надпочечников
- Полипы эндометрия
- Доброкачественная дисплазия молочной железы
- Воспалительные заболевания молочных желез
- Эндометриоз
- Сифилис
- Миома матки
Болезни в статье:
- E65-E68 Ожирение и другие виды избыточности питания
- L83 Acanthosis nigricans
- E10-E14 Сахарный диабет
- I10-I15 Болезни, характеризующиеся повышенным кровяным давлением
- E78 Нарушения обмена липопротеинов и другие липидемии
- L64 Андрогенная алопеция
- L70 Угри
- N85.0 Железистая гиперплазия эндометрия
- C54.1 Эндометрия
- N91.3 Первичная олигоменорея
- N91.1 Вторичная аменорея
- N97 Женское бесплодие
- L68.0 Гирсутизм
- G47.3 Апноэ во сне
- F41.2 Смешанное тревожное и депрессивное расстройство
- F50 Расстройства приема пищи
- F52 Сексуальная дисфункция, не обусловленная органическими нарушениями или болезнями
Фармгруппы в статье:
Оцените статью:
- Синдром Штейна-Левенталя
- Синдром поликистозных яичников
- Поликистоз яичников
- Синдром Стейна-Левенталя
- Склерокистозная болезнь яичников
- Синдром поликистозный яичников
- Штейна-Левенталя синдром
Жиросжигатель, стимулятор, ноотроп? Что известно о L-карнитине
Как работает L-карнитин: научные данные о спортивной добавке.
Опубликовано на сайте: 29.07.25 | Обновлено на сайте: 29.07.25
Полужирным шрифтом выделены лекарства, входящие в справочники текущего года. Рядом с названием препарата может быть указан ежегодный уровень индекса информационного спроса (показатель, который отражает степень интереса потребителей к информации о лекарстве).
поликистоз яичников
поликистоз яичников, синдроме поликистозных яичников, Синдром поликистозных яичников (СПКЯ), пациенток с поликистозными яичниками,





