- Эпидемиология
- Этиология, патогенез и факторы риска
- Факторы риска
- Классификация и стадирование неопухолевых и злокачественных заболеваний вульвы
- Клинические проявления рака вульвы
- Метастазирование рака вульвы
- Факторы прогноза
- Диагностика и лечение
- Лечение
- Отдаленные результаты лечения в зависимости от стадии заболевания
- Стадия 0 рака вульвы
- Стадия I рака вульвы
- Стадия II рака вульвы
- Стадия III рака вульвы
- Стадия IV рака вульвы
- Рецидивы рака вульвы
- Профилактика
C51 Злокачественное новообразование вульвы, МКБ-10
- C51.0 Большой срамной губы
- C51.1 Малой срамной губы
- C51.2 Клитора
- C51.8 Поражение вульвы, выходящее за пределы одной и более вышеуказанных локализаций
- C51.9 Вульвы неуточненной части
Отредактировано: 02.04.2024
д.м.н., проф. Кузнецов В.В., д.м.н., проф. Козаченко В.П., к.м.н. Коржевская Е.В.
ГУ РОНЦ им. Н.Н. Блохина РАМН
Эпидемиология. Этиология, патогенез и факторы риска. Классификация и стадирование неопухолевых и злокачественных заболеваний вульвы. Клинические проявления рака вульвы. Метастазирование рака вульвы. Диагностика и лечение. Профилактика
Несмотря на свою визуальную и мануальную диагностическую доступность, рак вульвы является одной из наиболее трудно излечимых злокачественных опухолей органов репродуктивной системы женщины. С одной стороны, это связано с особенностями кровоснабжения, иннервации и лимфатического оттока, а также топографической близостью смежных органов, с другой стороны — с высокой психосексуальной и физиологической значимостью наружных половых органов женщины для ее нормальной жизни. Из этого следует, что правильная оценка анамнеза, клинической симптоматики и рациональное построение диагностического процесса могут способствовать своевременному распознаванию рака этой локализации.
Эпидемиология
Результаты демографических исследований последних лет свидетельствуют о возросшей численности женского населения, переступившего рубеж менопаузы. В этой связи в современном обществе неуклонно растет интерес к проблемам здоровья и социальной адаптации женщин постменопаузального возраста. Средний возраст (68 лет) больных раком вульвы к моменту выявления заболевания — наибольший по сравнению с соответствующими показателями по другим опухолям органов репродуктивной системы. У девочек и женщин репродуктивного возраста рак вульвы встречается очень редко. По мере старения, особенно у лиц старше 70 лет, вероятность возникновения его увеличивается. У женщин старше 85 лет вероятность возникновения рака вульвы сравнивается с таковой для РШМ и РТМ. Таким образом рак вульвы — болезнь женщин пожилого и старческого возраста, большинство пациенток находится в возрастном диапазоне 60–75 лет.
Рак вульвы — относительно редко встречающаяся опухоль. В структуре заболеваемости злокачественными новообразованиями женских половых органов рак вульвы в России составляет 3–8% и занимает 4 ранговое место после РШМ, РТМ и РЯ.
В США рак вульвы составляет около 4% всех случаев рака женской репродуктивной сферы и 0,6% всех случаев рака у женщин. В 2001 г. в США диагностировано около 3600 случаев рака вульвы и около 800 смертей. В России и других экономически развитых странах Европы и Северной Америки заболеваемость раком вульвы примерно одинакова.
Этиология, патогенез и факторы риска
Этиология и патогенез рака вульвы изучены недостаточно. Патогенетический механизм развития различных звеньев заболевания чаще индуцируется гормональной перестройкой, происходящей в климактерическом и постменопаузальном периодах. Это в определенной мере и обусловливает тот факт, что рак вульвы возникает у женщин относительно пожилого возраста. Если учесть средний возраст больных неопухолевыми дистрофическими заболеваниями (НДЗ), 56 лет, становится понятно, что при выявлении ранних форм заболевания вульвы внимание должно быть обращено на возрастную группу 60 лет и старше. Средний возраст больных раком вульвы, находившихся на лечении в отделении онкогинекологии НИИ КО ГУ РОНЦ им. Н.Н. Блохина РАМН, составил 61,5±5,1 года.
Этиологическая классификация плоскоклеточного рака вульвы включает в себя по крайней мере 2 группы:
1. Меньшая группа — базалиоидные и бородавчатые опухоли, индуцированные человеческими папилломавирусами (HPV).
2. Бóльшая группа — плоскоклеточные раки, этиология которых неизвестна.
ДНК вируса папилломы человека обнаруживается у большинства женщин с остроконечными кондиломами, диспластическими изменениями покровного эпителия и раком вульвы, влагалища и шейки матки, что позволяет рассматривать HP-вирусную инфекцию как фактор развития рака этих локализаций. Таким образом в настоящее время имеются прямые доказательства (серологические и молекулярно-биологические) роли вирусной инфекции в этиологии рака вульвы.
Факторы риска
Существуют факторы, которые расцениваются как наиболее вероятные для развития рака вульвы:
— возраст: у 3/4 женщин это заболевание диагностируется в возрасте старше 50 лет, у 2/3 — в возрасте старше 70 лет;
— хроническое инфицирование папилломавирусом человека (HPV);
— инфицирование вирусом иммунодефицита человека (HIV);
— склерозирующий лишай;
— меланома или атипичные невусы на коже вне вульвы, передающиеся по наследству, повышают риск развития рака вульвы;
— интраэпителиальная неоплазия вульвы (VIN);
— рак гениталий другой локализации;
— ожирение;
— артериальная гипертензия;
— сахарный диабет;
— низкий социально-экономический статус;
— частая смена половых партнеров;
— курение.
Во многих случаях развитию рака вульвы предшествуют кондиломы или плоскоклеточная дисплазия. Папилломавирус человека (HPV) преобладает в этом ряду факторов риска.
Классификация и стадирование неопухолевых и злокачественных заболеваний вульвы
А. ;Неопухолевые дистрофические поражения кожи и слизистой оболочки:
— склерозирующий лишай (крауроз вульвы и атрофический вульвит);
— плоскоклеточная гиперплазия (лейкоплакия);
— смешанные формы (атрофические и гиперпластические изменения);
— другие дерматозы.
Международная медицинская ассоциация по изучению заболеваний вульвы в 1987 г. пришла к решению об обобщении упомянутых выше прежних названий гистогенетически родственных процессов под общим термином “Неопухолевые дистрофические поражения”.
Склерозирующий лишай (лихен)
Встречается главным образом у пожилых женщин (табл. 1).
Микроскопические признаки включают сглаживание и полное исчезновение эпидермальных отростков и субэпителиальную эозинофильную гомогенизацию дермы с выраженной редукцией или полным исчезновением эластичных волокон. Сопутствующее исчезновение пигмента создает картину “белого поражения вульвы” (лейкоплакии). Склерозирующий лишай, по современным данным, не имеет прямой генетической связи с опухолевыми процессами. Последние обычно непосредственно обусловлены дополнительно возникающими изолированными очагами плоскоклеточной гиперплазии.
Плоскоклеточная гиперплазия ;(лейкоплакия)
Расценивается в качестве неадекватной пролиферативной реакции эпителия вульвы на широкий круг раздражающих факторов (табл. 1). Может возникать в любом возрасте, но гораздо чаще отмечается в пре— и постменопаузальном периодах. Микроскопические признаки включают прежде всего акантоз и гиперкератоз. Папилломатозные структуры отсутствуют, что отличает плоскоклеточную гиперплазию от остроконечной кондиломы.
Таблица 1
Склерозирующий лишай и плоскоклеточная гиперплазия
| Признак | Патология | |
| Склерозирующий лишай | Плоскоклеточная гиперплазия | |
| Жалобы | Зуд | Зуд |
| Клинические и макроскопические проявления | Кожа тонкая, желтая, пергаментная, легко трескается | Кожа толстая, белого или желтого цвета |
| Уплотнение складок | Складки сморщиваются, иногда наблюдается пятнистость кожи | |
| Сужение входа во влагалище | Явного сужения во влагалище не наблюдается | |
| Микроскопические проявления | Эпидермис тонкий с нормальным или слегка утолщенным роговым слоем | Эпидермис утолщен в результате акантоза и гиперкератоза |
| Сосочковый слой сглажен | Сосочковый слой растянут | |
| Поверхностные слои собственно кожи отечны, а последний гиалинизирован | Отек не выражен | |
| Глубокие слои собственно кожи содержат клетки, свидетельствующие о хроническом воспалении; отсутствие подкожной жировой клетчатки | В глубоких слоях собственно кожи наблюдаются клетки, свидетельствующие о хроническом воспалении | |
| Атипия клеток встречается редко | Дисплазия наблюдается в 10% случаев | |
Дистрофические изменения смешанного типа
Отмечаются приблизительно в 15% случаев. Для этого вида изменений характерно, что некоторые участки кожи имеют признаки склерозирующего лишая, тогда как на других наблюдается типичная картина плоскоклеточной гиперплазии.
B. ;Интраэпителиальная неоплазия вульвы (VIN):
— I степень — легкая дисплазия (VIN1, легкая атипия);
— II степень — умеренная дисплазия (VIN2, умеренная атипия);
— III степень — тяжелая дисплазия (VIN3, тяжелая атипия);
— IV степень — карцинома ;in situ ;(VIN4).
До настоящего времени остается много спорных вопросов в трактовке фоновых и предраковых заболеваний. Опухоль часто развивается на фоне дистрофических процессов (крауроза и лейкоплакии). Однако истинным предраком является дисплазия, которую невозможно диагностировать без прицельной биопсии и гистологического исследования, т.к. клиническая симптоматика в большинстве случаев отсутствует. Под маской клинически определяемых неопухолевых дистрофических поражений (крауроза и лейкоплакии) могут скрываться предраковые заболевания (VIN2 ;и VIN3) и начальные формы рака вульвы. Длительное консервативное лечение больных с неопухолевыми дистрофическими заболеваниями вульвы без гистологического исследования является очень распространенной ошибкой и приводит к запоздалой диагностике. Это особенно важно для больных с клиническими проявлениями плоскоклеточной гиперплазии (лейкоплакии), когда назначение мазей и кремов с эстрогенами, кортикостероидами и анальгезирующими средствами, спиртоновокаиновые блокады нервных окончаний наружных гениталий купируют боль и зуд. Почувствовав облегчение, больные перестают посещать врача, а через какое-то время симптомы возобновляются, и развивается злокачественная опухоль с метастазами.
Отечественные онкологи считают, что тяжелые дисплазии чаще развиваются на фоне неопухолевых дистрофических поражений вульвы, в частности, склерозирующего лишая (крауроз вульвы, атрофический вульвит), плоскоклеточной гиперплазии (лейкоплакия) и других дерматозов. Последние имеют неблагоприятное патогенетическое значение, обусловленное обширностью поражения и мультифокальностью опухолевой трансформации покровного эпителия вульвы. Дисплазии на фоне неизмененной кожи половых губ у молодых женщин редко переходят в инвазивный рак вульвы в связи с возможной спонтанной регрессией.
В настоящее время широко применяется новая классификация злокачественных опухолей женских половых органов, которая создавалась с учетом классификаций, применяемых международной Федерацией гинекологов и акушеров (FIGO, 1989 г., уточнена в 1990 г.), Национальными комитетами TNM (1998 г.) и Американским противораковым союзом (AJCC). Определение категорий TNM соответствует стадиям, применяемым FIGO, поэтому для сравнения приведены обе классификации. Согласно этим классификациям существуют 4 стадии рака вульвы в зависимости от распространенности опухолевого процесса.
Клиническая классификация TNM
Критерий T ;(первичная опухоль)
Tx ;— недостаточно данных для оценки первичной опухоли;
T0 ;— первичная опухоль не определяется;
Tis ;— карцинома ;in situ ;(преинвазивная карцинома);
T1 ;— опухоль ограничена вульвой и/или промежностью, ≤2 см в наибольшем измерении;
T1A ;— глубина инвазии стромы ≤1 мм*;
T1B ;— глубина инвазии стромы >1 мм*;
T2 ;— опухоль ограничена вульвой и/или промежностью, >2 см в наибольшем измерении;
T3 ;— опухоль любого размера, распространяющаяся на нижнюю часть уретры и/или влагалище, или анальное кольцо;
T4 ;— опухоль любого размера, распространяющаяся на любую из следующих cтруктур: на слизистую оболочку верхней части мочеиспускательного канала и/или мочевого пузыря, и/или прямой кишки и/или опухоль фиксирована к костям таза.
Состояние регионарных лимфатических узлов (N)**
Nx ;— недостаточно данных для оценки состояния регионарных лимфатических узлов;
N0 ;— нет метастазов в регионарных лимфатических узлах;
N1 ;— метастазы в регионарных лимфатических узлах с одной стороны;
N2 ;— метастазы в регионарных лимфатических узлах с двух сторон;
Критерий M ;(отдаленные метастазы)
Mx ;— недостаточно данных для определения отдаленных метастазов;
M0 ;— нет отдаленных метастазов;
M1 ;— отдаленные метастазы (включая метастазы в тазовых лимфатических узлах);
М1A ;— метастазы в тазовых лимфатических узлах;
М1B ;— другие отдаленные метастазы.
*Глубина инвазии определяется как измерение опухоли от эпителиально-стромального соединения наиболее поверхностного сосочка дермы до самой глубокой точки инвазии.
**При гистологическом анализе материала паховой лимфаденэктомии должно быть исследовано не менее 6 лимфатических узлов; при тазовой лимфаденэктомии — не менее 10 лимфатических узлов.
Группировка по стадиям (FIGO и TNM) представлена в таблице 2.
Таблица 2
Группировка по стадиям (FIGO и TNM)
| Стадии | T | N | M |
| Стадия 0 | Tis | N0 | M0 |
| Стадия IA | T1A | N0 | M0 |
| Стадия IB | T1B | N0 | M0 |
| Стадия II | T2 | N0 | M0 |
| Стадия III | T1 | N1 | M0 |
| T2 | N1 | M0 | |
| T3 | N0 | M0 | |
| T3 | N1 | M0 | |
| Стадия IVA | T1 | N2 | M0 |
| T2 | N2 | M0 | |
| T3 | N2 | M0 | |
| T4 | любая N | M0 | |
| Стадия IVB | любая T | любая N | M1 |
По распространенности опухолевого процесса больные в нашей клинике разделялись так: TisN0M0 ;— 5,5%, T1N0M0 ;— 24,2%, в т.ч. T1AN0M0 ;— 5,5%, T1BN0M0 ;— 18,7%, T2N0M0 ;— 39,6%, T2N1M0 ;— 8,8%, T3N0M0 ;— 4,4%, T3N1M0 ;— 13,2%, T2N2M0 ;— 2,2%, T3N2M0 ;— 2,2%.
Вульва является наружным анатомическим отделом полового тракта женщины. В структуре ее тканей широко представлены различные дериваты кожи, железистые и меланоцитарные элементы. Отсюда значительное многообразие встречающихся злокачественных опухолей. Вместе с тем клинически наиболее значимыми гистологическими формами являются злокачественные новообразования, развивающиеся из покровного плоского эпителия наружных половых органов. Плоскоклеточный рак различной степени дифференцировки встречается у 90% больных злокачественными опухолями вульвы.
Морфологическая классификация предопухолевых заболеваний и злокачественных опухолей вульвы (ВОЗ, МКБ-О, 1990)
I. Предопухолевые заболевания и злокачественные опухоли эпителиального происхождения:
A. Изменения плоского эпителия:
1. Дисплазия вульвы и рак ;in situ ;(VIN, вульварная интраэпителиальная неоплазия):
a) легкая дисплазия (VIN1);
b) умеренная дисплазия (VIN2);
c) тяжелая дисплазия (VIN3);
d) рак ;in situ ;(VIN4).
2. Плоскоклеточный рак:
a) ороговевающий;
b) неороговевающий;
c) базалиоидный;
d) веррукозный;
e) кондиломатозный;
f) другие формы.
3. Базально-клеточный рак.
B. Изменения железистого эпителия:
1. Экстрамамиллярный рак Педжета.
2. Рак бартолиневой железы:
a) аденокарцинома;
b) плоскоклеточный рак;
c) аденокистозный рак;
d) железисто-плоскоклеточный рак;
e) переходно-клеточный рак.
3. Рак из эктопической ткани молочной железы.
4. Рак потовых желез.
5. Другие аденокарциномы.
II. Злокачественные опухоли мягких тканей:
A. Рабдомиосаркомы.
B. Агрессивная ангиомиксома.
C. Лейомиосаркома.
D. Выбухающая дерматофибросаркома.
E. Злокачественная фиброзная гистиоцитома.
F. Эпителиоидная саркома.
G. Злокачественная шваннома.
H. Злокачественная гемангиоэндотелиома.
I. Саркома Капоши.
J. Гемангиоперицитома.
K. Липосаркома.
L. Альвеолярная саркома мягких тканей.
III. Другие злокачественные опухоли:
A. Меланома.
B. Гемобластозы.
C. Опухоль желточного мешка.
D. Опухоль из клеток Меркеля.
E. Метастатические опухоли.
Метастатические опухоли имеют своим первичным источником чаще всего плоскоклеточный рак шейки матки. Далее в порядке убывания стоят рак эндометрия, мочевого пузыря и уретры. Реже в вульве могут развиваться метастазы рака влагалища, молочных желез, яичников, почек, меланомы кожи, хориокарциномы, рака бронхов, лимфомы.
Клинические проявления рака вульвы
Признаки и симптомы раннего инвазивного плоскоклеточного рака вульвы похожи на таковые при VIN. Отличия проявляются при увеличении инвазии опухоли и дальнейшем прогрессировании. Наиболее частыми симптомами болезни являются раздражение или зуд вульвы, наличие опухоли, болезненной язвы и боли в области вульвы, носящие длительный рецидивирующий и упорный характер. Наиболее общими симптомами являются опухоли в виде бородавки и/или ссадины ярко-розового, красного или белого цвета. Участок вульвы может казаться бледным и негладким на ощупь. Около половины больных раком вульвы жалуются на постоянный и усиливающийся зуд в этой области. Реже первыми проявлениями заболевания служат кровянистые или гнойные выделения, увеличение паховых лимфатических узлов. Некоторые предъявляют жалобы на боль, жжение в области вульвы, болезненное мочеиспускание. Еще одним признаком является незаживающая более месяца язва на вульве.
Таким образом клинические проявления рака вульвы различны и зависят от фона, на котором развивалось заболевание.
Если опухоли вульвы ;не предшествовали неопухолевые дистрофические процессы, в ранних стадиях заболевания симптомы выражены незначительно и проявляются возникновением дискомфорта (зуд, жжение), а затем развитием небольшой язвы. По мере прогрессирования болезни выраженность симптомов усиливается. При инфильтрации подлежащих тканей появляются боли в области промежности, рези и жжение при мочеиспускании, особенно когда имеется инфильтрация наружного отверстия мочеиспускательного канала. Образование значительной по размерам опухоли приводит к появлению обильных зловонных выделений, может возникнуть кровотечение.
При развитии рака ;на фоне неопухолевых дистрофических процессов ;ведущим симптомом является зуд, который имеет приступообразный характер и усиливается ночью.
Первые симптомы рака вульвы напрямую зависят от локализации и анатомической формы роста опухоли. Наиболее часто плоскоклеточный рак локализуется на большой половой губе. Второй анатомической структурой по частоте опухолевого поражения являются малые половые губы. Значительно реже местом локализации первичной опухоли являются клитор, уретра и промежность. При распространенных процессах установить первичную локализацию опухоли не представляется возможным. У 5–10% больных уже при первичном обращении можно наблюдать 2–3 и более определяемых клинически опухолей в различных отделах наружных половых органов. Известен ;феномен зеркально отраженных опухолей вульвы ;на малых половых губах, в результате чего образуется их характерная бабочкообразная форма.
Для рака вульвы характерными формами анатомического роста опухоли являются экзофитные и эндофитные язвенные новообразования. Значительно реже встречаются опухоли, отличающиеся инфильтративным ростом с отечным компонентом. В таких случаях опухоль инфильтрирует всю поверхность наружных половых органов и отличается крайне агрессивным клиническим течением. Раннее развитие лимфогенных метастазов, распространение на влагалище, уретру и промежность, прорастание в мочевой пузырь, анальное кольцо и прямую кишку — характерные признаки агрессивности подобных форм злокачественных новообразований вульвы. Кроме прорастания в смежные органы и лимфогенного метастазирования в регионарные лимфатические узлы, при раке вульвы можно наблюдать отдаленные гематогенные метастазы в легкие, печень, кости. Местно-распространенные формы плоскоклеточного рака вульвы составляют подавляющее большинство наблюдений, а гематогенные метастазы достаточно редки.
Метастазирование рака вульвы
Ключом к решению проблемы индивидуального лечения при раке вульвы является понимание механизма лимфатического оттока от вульвы и различных путей метастазирования (рис. 1).
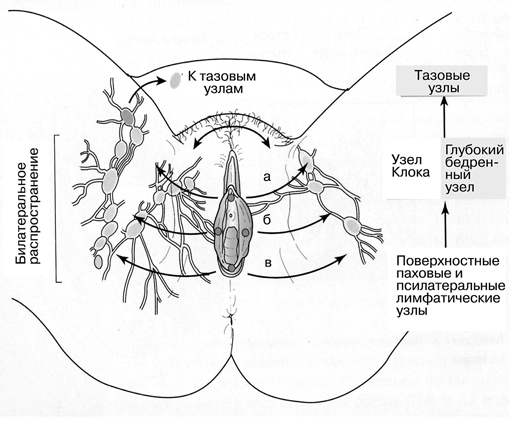
Рисунок 1. Основные направления метастазирования лимфы:
а — из области клитора — во внутритазовые узлы с обеих сторон через над— и подлобковые лимфатические сосуды; б —из передних отделов — в поверхностные паховые лимфоузлы с той же стороны и через пресимфизиальное сплетение на противоположную сторону; в — из задних отделов — непосредственно в поверхностные паховые лимфоузлы на той же стороне
Частое и быстрое метастазирование обусловлено богато развитой лимфатической сетью, которая охватывает всю вульву и отводит лимфу в лимфатические узлы. В то время как отток лимфы из задних отделов вульвы происходит непосредственно в поверхностные паховые лимфатические узлы на той же стороне, отток ее из передних отделов происходит в те же лимфатические узлы и, кроме того, через пресимфизиальное сплетение в поверхностные паховые лимфатические узлы противоположной стороны. Отток лимфы из клитора в основном происходит во внутритазовые узлы с обеих сторон через надлобковые и подлобковые лимфатические сосуды.
Ведущим признаком клинической агрессии опухоли является наличие метастазов опухоли в регионарные лимфатические узлы — паховые, бедренные (глубокие паховые) и особенно в подвздошные. Крайне злокачественным течением отличаются опухоли клитора, когда нарушается этапность лимфогенного метастазирования. Лимфогенные метастазы наблюдаются уже на ранних стадиях рака вульвы. Частота метастазов рака вульвы в лимфатические узлы пахово-бедренного коллектора у операбельных больных I-III стадий составляет от 30 до 50%, на первом этапе метастазами поражаются поверхностные паховые лимфатические узлы, на втором — глубокие, вокруг магистральных бедренных сосудов. Особое клиническое значение придается метастазам в проксимальную группу глубоких паховых (бедренных) лимфатических узлов (Клоке — Розенмюллера — Пирогова), за которыми метастазы развиваются в подвздошных и запирательных лимфатических узлах. В группе подвздошных лимфатических узлов чаще всего метастазы выявляются в наружных подвздошных. Подобная ситуация является критической для больных раком вульвы. Ситуация становится фатальной при метастазах в поясничные лимфатические узлы. При раке клитора у 10–30% больных можно наблюдать изолированные метастазы опухоли в подвздошные лимфатические узлы при интактных лимфатических узлах пахово-бедренного коллектора. Метастазирование бывает перекрестным, т.е. контралатеральным по отношению к локализации опухоли. Гематогенные метастазы при раке вульвы наблюдаются, как правило, при наличии метастазов в подвздошных, парааортальных и паракавальных лимфатических узлах.
Факторы прогноза
Прогноз больных раком вульвы напрямую зависит от массивности лимфогенной диссеминации опухоли. Частота лимфогенного метастазирования нарастает при:
— увеличении глубины инвазии опухоли;
— снижении степени ее дифференцировки;
— обнаружении раковых эмболов в просвете лимфатических и кровеносных сосудов;
— анеуплоидных новообразованиях.
Риск метастазирования в лимфатические узлы практически равен нулю при глубине стромальной инвазии опухоли менее 2 мм; 20% — при глубине инвазии более 2 мм и около 40% — при глубине инвазии более 4 мм.
Значительно больше шансов излечить больную раком вульвы с переходом опухоли на нижнюю треть влагалища или дистальную часть уретры (Т3) без метастазов в регионарные лимфатические узлы, чем больную, у которой имеется одиночная опухоль размером до 2 см (Т1) со множественными метастазами в ;лимфатические узлы пахово-бедренного треугольника.
Факторами прогноза для лимфогенного метастазирования являются:
— клиническая оценка лимфатических узлов, возраст;
— степень дифференцировки опухоли;
— стадия, первичный размер опухоли;
— глубина стромальной инвазии опухоли;
— локализация опухоли.
Однако при ;поражении лимфатических узлов ;общая выживаемость приближается к 50–60%. Около 30% оперированных больных имеют поражение лимфатических узлов. Больные без метастазов в лимфатические узлы и опухолью не более 2 см имеют 5-летнюю выживаемость 98%. В то же время при поражении 3 и более лимфатических узлов с одной стороны или 2 и более лимфатических узлов с двух сторон 5-летняя выживаемость снижается до 29%.
Размер опухоли. У 92% больных, которые живы 5 и более лет без рецидива и метастазов, размеры опухоли не превышают 2 см. Худшим прогнозом отличаются опухоли, наибольший размер которых превышает 2 см: 5-летняя выживаемость в этой группе больных составляет только 42%.
Определенное прогностическое значение имеет ;гистологическое строение опухоли. Более благоприятное клиническое течение наблюдается при плоскоклеточном ороговевающем раке. У больных плоскоклеточным неороговевающим раком в 1,5 раза чаще возникают метастазы в регионарных лимфатических узлах, что ухудшает прогноз заболевания. Существует определенная клиническая тенденция к ухудшению отдаленных результатов лечения у больных плоскоклеточным неороговевающим раком вульвы. При анализе 5-летней выживаемости больных раком вульвы в зависимости от формы анатомического роста опухоли наиболее неблагоприятной и одновременно относительно редко встречающейся оказалась эндофитная, язвенная форма. Лучшим прогнозом характеризуются экзофитно растущие опухоли, промежуточное положение занимают опухоли, имеющие смешанную форму анатомического роста. У больных раком вульвы, в зависимости от анатомической формы роста при эндофитных, экзофитных и смешанно растущих опухолях, 5-летняя выживаемость составляет 40; 60,9; 50% соответственно.
Заслуживают внимания работы по оценке прогностической значимости точечных мутаций гена ;p53, а также повышения сывороточного уровня бета-субъединицы ХГ у больных раком вульвы, исследования антигена плоскоклеточного рака (SCC) и РЭА как маркеров рака вульвы. Определение серологических уровней SCC и РЭА полезно не только для дооперационной оценки риска возникновения метастазов в лимфатические узлы, но также и для диагностирования рецидива заболевания.
Диагностика и лечение
Для объективной оценки состояния женщины используется комплекс единых и наиболее информативных методов исследования:
— гинекологический осмотр;
— вульвоскопия и расширенная вульвоскопия;
— цитологическое исследование;
— морфологическое исследование (биопсия опухоли и пункционная биопсия паховых лимфатических узлов);
— бактериоскопическое и бактериологическое исследования.
Существенным моментом диагностики является ;методика взятия материала для цитологического и морфологического исследований. При цитологическом исследовании часто не удается верифицировать диагноз, поскольку к нейродистрофическому фону нередко присоединяется воспалительная реакция. Иногда множественные очаги лейкоплакии, находясь в разных стадиях развития, сливаются, образуя единый белесоватый покров, что создает определенные трудности при диагностике рака в плане выбора места биопсии. Оптимальным методом диагностики является морфологическое исследование.
Для уточнения степени распространения опухоли рутинно применяют лучевые (рентгенологические и ультразвуковые) методы диагностики. По показаниям выполняют уретро— и цистоскопию, экскреторную урографию, радиоизотопное исследование почек, ректороманоскопию, КТ, радиоизотопную лимфографию, рентгенографию грудной клетки. Если необходимо, выполняют биопсию слизистой мочевого пузыря и/или прямой кишки.
Лечение
По данным отечественных и зарубежных авторов, общими принципами тактики ведения больных раком вульвы являются:
— хирургическое лечение при I стадии заболевания;
— комбинированное (хирургическое и лучевое) при II и III стадиях;
— индивидуальный подход (сочетание лучевых, лекарственных и хирургических методик) при IV стадии и рецидивах заболевания.
Только в случаях абсолютных противопоказаний к хирургическому вмешательству лучевая терапия может применяться как самостоятельный метод лечения в сочетании или без химиотерапии.
Типы хирургических вмешательств
Хирургическое лечение является методом выбора практически у каждой больной I-II стадиями рака вульвы.
Для хирургического лечения рака вульвы разработано несколько типов оперативных вмешательств. При одиночных экзофитных опухолях вульвы, размер которых в наибольшем диаметре не превышает 2 см, локализованных на одной из малых или больших половых губ, при отсутствии пальпируемых паховых лимфатических узлов у женщин молодого возраста хирургическое вмешательство на первом этапе операции может быть ограничено ;ножевым иссечением опухоли ;в пределах здоровых тканей. При этом линия разреза должна проходить не менее чем на 1 см от визуально определяемого края опухоли по всей ее окружности. Окончательный объем хирургического вмешательства определяется хирургом в зависимости от результатов срочного гистологического исследования. Операция может быть ограничена только иссечением образования при глубине инвазии опухоли в строму до 1 мм. При большей инвазии опухоли следует выполнить ;вульвэктомию. Рекомендации отдельных авторов о возможности ограничения объема хирургического вмешательства в виде только иссечения опухоли при глубине инвазии более чем 1 мм не выдерживают критики из-за нарастания риска метастатического поражения паховых лимфатических узлов, которые при микрометастазах могут не пальпироваться. Прямыми показаниями к ;вульвэктомии без паховой лимфаденэктомии ;являются: мультицентрический рост опухоли, развитие опухоли на фоне дистрофических изменений всей поверхности вульвы или ее локализация в периклиторальной области.
При прочих равных условиях, когда опухоль локализуется в складке между большой и малой половой губами, объем хирургического вмешательства может быть ограничен удалением половых губ только на стороне поражения, т.е. ;гемивульвэктомией. Операции иссечения опухоли, гемивульвэктомия, имеют достаточно четкие показания и относятся к щадящим хирургическим методам лечения рака вульвы. При перечисленных видах хирургических вмешательств нет необходимости в глубоком иссечении подлежащих тканей.
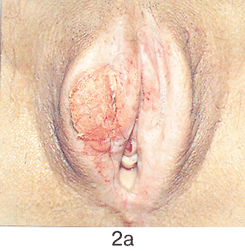
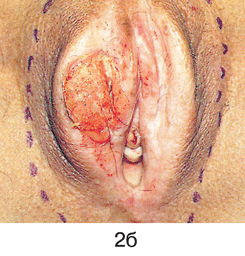
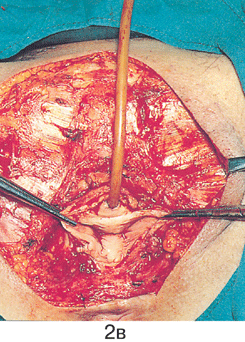
Простая вульвэктомия ;(см. рис. 2 на цветной вклейке) выполняется из лаврообразного разреза, окаймляющего снаружи вульву таким образом, что верхняя точка разреза находится на 1,5–2 см выше клитора, нижняя — на таком же расстоянии от задней спайки вульвы. Иссекаются кожа и слизистые покровы вульвы, а также 1–1,5 см подлежащей жировой клетчатки. После завершения внешнего разреза и проведения промежуточного гемостаза выполняется внутренний разрез, контур которого повторяет овал преддверия влагалищной трубки. Верхняя граница внутреннего разреза должна проходить на расстоянии не менее 1 см выше наружного отверстия уретры, нижняя — по задней стенке вульвы. В глубине подлежащей жировой клетчатки разрезы сходятся и удаляется послеоперационный препарат. Гемостаз обеспечивается электрокоагуляцией и наложением узловых кетгутовых или синтетических рассасывающихся швов на подкожную жировую клетчатку. На кожу и стенку влагалища накладываются съемные синтетические узловые швы, что обеспечивает сведение краев операционной раны и позволяет добиться определенного косметического эффекта. При наложении швов необходимо избегать излишнего натяжения тканей. В противном случае в связи с рубцеванием могут возникнуть деформация дистальной части уретры и сужение входа во влагалище.
 ;
; ;
; ;
; ;
;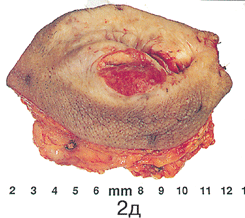
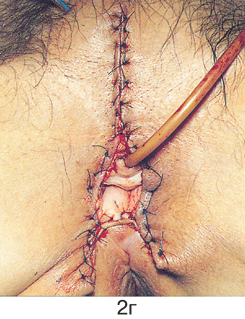
Рисунок 2. Простая вульвэктомия:
а – опухоль до операции; б – лаврообразный разрез; в – этап операции, макропрепарат удален; г – послеоперационная рана; д – макропрепарат
В настоящее время наиболее распространенной и достаточно адекватной операцией при инвазивном раке вульвы является ;расширенная вульвэктомия, которая по показаниям выполняется в 2 различных вариантах:
1. Расширенная вульвэктомия выполняется из 3 разных, не соединяющихся между собой разрезов. Послеоперационный материал состоит из 3 отдельно удаленных блоков тканей — вульвы и 2 последовательно иссеченных из пахово-бедренных областей кожно-жировых лоскутов.
2. В ходе операции разрезы в области вульвы и паховых областей соединяются между собой. Таким образом хирург проводит удаление вульвы и тканей пахово-бедренной зоны одним блоком, что при опухолях вульвы, имеющих значительное местно-регионарное распространение, имеет принципиальное значение. При расширенной вульвэктомии из 3 разрезов операция начинается с поэтапного иссечения анатомических структур пахово-бедренных областей. На 2 см ниже и параллельно паховой связке выполняется лаврообразный разрез кожи длиной 8–10 см и шириной от 2 до 4 см. Медиальная точка разреза не доходит до лобковой зоны, а латеральная находится в таком же соотношении к передней верхней ости подвздошной кости. Из выполненного разреза создается хороший доступ к бедренному (скарповскому) треугольнику (trigonum femorale). Края созданной операционной раны легко растягиваются. Обнаженное операционное поле образует треугольник, отправными точками которого являются передняя верхняя ость подвздошной кости (spina iliaca anterior superior), лонный бугорок (tuberculum pubicum) и вершина скарповского треугольника. Линейные границы операционного поля составляют сверху паховая связка (lig. inguinale), латерально портняжная мышца (m. sartorius) и медиально длинная приводящая мышца бедра (m. adductor longus). Интересы хирурга и прогноз больной “заложены” в этой анатомической зоне. Все хирургические манипуляции в этой области должны осуществляться только острым путем, а удаляемые ткани иссекаются только единым блоком. Верхний пласт удаляемых тканей включает подкожную жировую клетчатку и поверхностные паховые лимфатические узлы (nodi lymphatici inguinales superficiales), которые находятся между поверхностным и глубоким листками поверхностной фасции бедра. Нижний пласт подлежащих удалению тканей включает в себя глубокие паховые (бедренные) лимфатические узлы (nodi lymphatici inguinales profundi) с окружающей клетчаткой. Описанные структуры располагаются между поверхностным и глубоким листками широкой фасции бедра (fascia lata). Глубокий листок широкой фасции бедра интимно покрывает мышцы передней поверхности бедра и магистральные бедренные сосуды с одноименным нервом. Во время операции последовательно в пределах обозначенной анатомической зоны пересекаются все указанные структуры. Отсепаровка тканей осуществляется от периферии к центру операционного поля, где располагаются магистральные бедренные сосуды. Этот этап операции Я.В. Бохман назвал “формированием фасциального конверта”. При этом пересекают и лигируют сосуды, обеспечивающие кровоснабжение этой зоны: поверхностные, огибающие подвздошную кость (aa. et vv. circumflexae iliacae superficiales), ветви гребешково-приводящих и нижних наружных срамных артерий и вен (aa. et vv. pudendae externae), большую подкожную вену (v. saphena magna). Последнюю пересекают дважды — у дистальной вершины операционного треугольника и места впадения в бедренную вену. Таким образом резецированный участок большой подкожной вены удаляется в блоке иссеченных тканей. Перед удалением операционного препарата следует убедиться в том, что в удаляемый блок тканей включен лимфатический узел или несколько узлов, которые запирают бедренный канал (Клоке — Розенмюллера — Пирогова). После удаления операционного препарата на мышечном дне обнаженного скарповского треугольника визуализируется только сосудисто-нервный бедренный пучок. Послойное ушивание раны проводится после тщательного гемостаза и дренирования, что в определенной степени снижает образование лимфатических затеков и инфицирование раны. Объем лимфаденэктомии может быть расширен. Показанием к расширению лимфодиссекции являются только метастазы рака вульвы в лимфатические узлы пахово-бедренного коллектора. В сомнительных случаях выполняется срочное гистологическое исследование отдельных подозрительных на метастатическое поражение лимфатических узлов. Особое внимание уделяется состоянию лимфатического узла Клоке — Розенмюллера — Пирогова, который является самым дистальным подвздошным лимфатическим узлом тазовой области. Его метастатическое поражение служит прямым показанием к тазовой лимфаденэктомии. Таким образом, этот лимфатический узел играет роль “сторожевого”.
Лимфаденэктомия подвздошных и обтураторных лимфатических узлов ;может быть выполнена из 3 доступов. Все 3 доступа предполагают выполнение внебрюшинной лимфаденэктомии.
Отсекается паховая связка (lig. inguinale) от места ее прикрепления к верхней передней ости подвздошной кости (spina iliaca anterior superior), или разрез выполняется выше и параллельно паховой связке, или косой разрез в подвздошной области, нижней точкой которого является середина паховой связки. При 2 последних доступах рассекается апоневроз наружной косой мышцы живота (m. obliquus externus abdominis), обнажается париетальная брюшина. Смещение последней в медиальную сторону позволяет раскрыть забрюшинное пространство и визуализировать большую поясничную мышцу (m. psoas major), магистральные подвздошные сосуды, лимфатические узлы с окружающей клетчаткой таза. Далее производят типичную одноблочную лимфодиссекцию наружных, внутренних подвздошных и запирательных лимфатических узлов с окружающей клетчаткой таза на стороне метастатического поражения паховых лимфатических узлов.
При расширенной вульвэктомии по второму варианту удаление вульвы и пахово-бедренная лимфаденэктомия производятся одним блоком с кожей и подкожной жировой клетчаткой лобковой области, при необходимости с резецированной дистальной частью уретры, нижней третью влагалищной трубки, кожей и мягкими тканями промежности. Показанием к выбору второго варианта расширенной вульвэктомии является значительное местно-регионарное распространение злокачественной опухоли. Принцип одноблочного удаления операционного препарата достигается благодаря дугообразному разрезу, который соединяет передние верхние ости подвздошных костей. Самой нижней точкой этого разреза служит верхний край лонного сочленения. Одновременно это и хирургический ориентир для определения верхней границы вульвэктомии. Два полулунных, по пахово-бедренным складкам сходящихся на промежности разреза завершают анатомические границы блока удаляемых тканей. После удаления операционного препарата на дне раны определяются симфиз, седалищно-пещеристая мышца (m. ischiocavernosus), глубокая поперечная мышца промежности (m. transversus perinei profundus) с фасцией, которая ее покрывает, луковично-губчатая мышца (m. bulbospongiosus) и анатомические структуры скарповских треугольников с магистральными бедренными сосудами и одноименными нервами. Расширенную вульвэктомию в любом варианте предпочтительно выполнять электроножевым способом, что способствует снижению кровопотери и повышает абластичность операции. На этом этапе операции следует ушить отверстие бедренного канала, а при значительном обнажении магистральных бедренных сосудов провести их укрытие портняжной мышцей. Тщательный гемостаз и дренирование составляют необходимые условия профилактики образования ложных лимфатических кист, затеков и нагноения раны. Кожные швы накладываются на расстоянии 2–2,5 см друг от друга, что позволяет избежать излишнего натяжения тканей и их деформации.
В послеоперационном периоде необходим тщательный уход за операционной раной. Отведение мочи проводится через постоянный катетер Фолея в течение 7–8 дней. Тщательная подготовка кишечника перед операцией, парентеральное питание и щадящая диета позволяют в первые несколько суток избежать инфицирования операционной раны, что, в сочетании с адекватной антибиотикопрофилактикой, позволяет добиться первичного заживления у 50–60% больных.
Осложнения
И все-таки наиболее частыми ранними осложнениями после расширенной вульвэктомии остаются раневая инфекция, некроз кожных краев раны и несостоятельность кожных швов, которые отмечаются примерно у 40–50% больных.
Далее по частоте встречаемости следуют:
— лимфатические затеки с образованием ложных лимфатических кист,
— тромбозы глубоких вен,
— инфекции мочевыводящих путей,
— кровотечения.
Самым частым поздним осложнением, которое развивается в той или иной степени у 65–70% больных, является ;лимфостаз нижних конечностей. При IV клинической стадии рака вульвы (T4N1–2M0) у больных молодого возраста, когда имеется прорастание опухоли в проксимальную часть уретры, мочевой пузырь, ректовагинальную перегородку, анус или прямую кишку, радикальное хирургическое лечение возможно только при выполнении того или иного типа ;тазовой экзентерации, которая дополняется расширенной вульвэктомией. Больным преклонного возраста выполнение хирургических вмешательств подобного объема просто невозможно в связи с высоким риском летальных исходов. Альтернативой радикальному хирургическому лечению этой категории больных служат лучевое или химиолучевое лечение, которые индивидуально дополняются паллиативными операциями.
В подавляющем большинстве наблюдений больные III стадией рака вульвы получают комбинированное лечение, когда операция выполняется до или после лучевой терапии. При прорастании опухоли в проксимальную часть уретры, мочевой пузырь, ректовагинальную перегородку, прямую кишку могут выполняться различные типы экзентерации тазовых органов в сочетании с расширенной вульвэктомией.
Отдаленные результаты лечения в зависимости от стадии заболевания
Стадия 0 рака вульвы
Простая вульвэктомия дает практически 100%-ную 5-летнюю выживаемость, но рак вульвы на данной стадии диагностируется редко. Местное использование лекарственной терапии не является надежным методом выбора для лечения стадии 0 рака вульвы. Выбор метода лечения зависит от распространенности процесса.
Методы выбора
1. Широкое локальное иссечение, лечение лазером или их комбинация.
2. Вульвэктомия с/без пересадки лоскута ткани.
3. Химиотерапия ;фторурацилом ;(5% мазью) местно (положительный результат в 50–60%) (Malfetano J.H. et. al., 1985).
По результатам ГУ РОНЦ им. Н.Н. Блохина РАМН излечение достигнуто у 56% больных раком вульвы I-IV стадий; у 100% больных внутриэпителиальным раком.
Стадия I рака вульвы
Радикальная вульвэктомия дает 5-летнюю выживаемость до 90%.
Методы выбора
1. Для микроинвазивного рака (инвазия до 1 мм), не связанного с тяжелой дисплазией вульвы, показано широкое (5–10 мм) иссечение. Для всех других вариантов рака вульвы стадии I должно быть выполнено радикальное локальное иссечение с односторонней лимфаденэктомией на стороне локализации опухоли при клинически неопределяемых лимфатических узлах и без диффузной тяжелой дистрофии вульвы (Stehman F.B. et al., 1992). Другие варианты рака вульвы стадии I — это опухоль до 2 см в диаметре с инвазией до 5 мм и клинически без признаков метастатического поражения регионарных лимфатических узлов. Местные рецидивы заболевания возникают в 7% случаев после локального радикального иссечения по сравнению с 6% после радикальной вульвэктомии.
2. Радикальная вульвэктомия с двусторонней пахово-бедренной лимфаденэктомией. Травматичность этих операций может быть уменьшена за счет изолированного удаления паховых лимфатических узлов или односторонней паховой лимфаденэктомии, что является методом выбора для ранних форм рака вульвы. Лучевая терапия на паховую область при клинически интактных лимфатических узлах (N0) является альтернативой паховой лимфодиссекции для тех больных, которые отказываются от проведения паховой лимфодиссекции или имеют медицинские противопоказания.
3. Некоторой части больных, которым не показана радикальная вульвэктомия из-за локализации или распространенности процесса, проводится сочетанная лучевая терапия.
По данным ГУ РОНЦ им. Н.Н. Блохина РАМН, 90,9% больных I стадией наблюдаются после проведенного лечения в течение 5 и более лет без признаков рецидива болезни.
Стадия II рака вульвы
Радикальная вульвэктомия и двусторонняя пахово-бедренная лимфаденэктомия являются стандартным методом лечения и дают 80–90% 5-летней выживаемости в зависимости от размера первичной опухоли.
Методы выбора
1. Радикальная вульвэктомия с двусторонней пахово-бедренной лимфаденэктомией. Линия резекции должна проходить не менее, чем в 10 мм от опухоли. Травматичность этих операций может быть уменьшена вследствие изолированного удаления паховых лимфатических узлов. Лучевая терапия на паховые лимфатические узлы при N0 ;клинической стадии является альтернативой паховой лимфаденэктомии для женщин, которые отказываются или имеют медицинские противопоказания для проведения паховой лимфаденэктомии.
2. Для тех пациенток, которым невозможно проведение радикальной вульвэктомии из-за локализации или распространенности опухолевого процесса и сопутствующей патологии, проводится радикальная лучевая терапия.
По данным ГУ РОНЦ им. Н.Н. Блохина РАМН, излечение достигнуто у 52,7% больных II стадией заболевания.
Стадия III рака вульвы
Радикальная вульвэктомия с пахово-бедренной лимфаденэктомией является стандартным лечением. Вовлечение лимфоузлов в опухолевый процесс — определяющий фактор выживаемости. Показатели 5-летней выживаемости больных с односторонним единичным метастатическим поражением лимфатических узлов составляют 70%, снижаясь до 30% для больных с 3 и более метастатическими лимфатическими узлами с одной стороны (Russell A.H. et al., 1992). По данным ГУ РОНЦ им. Н.Н. Блохина РАМН, 5-летняя выживаемость больных с односторонним поражением пахово-бедренных лимфатических узлов (N1) в сочетании с местным распространением опухоли (T2) составила 50%, а при T — только 16,7%.
Результаты комбинированного лечения больных III стадией заболевания, когда распространенность опухолевого процесса выражается символами T1–2N1M0, в среднем на 15–20% превосходят таковые при проведении только лучевой терапии.
Методы выбора
1. Радикальная вульвэктомия с пахово-бедренной лимфаденэктомией. Лучевая терапия на паховые и тазовые лимфатические узлы показана, если определяются метастазы в паховые лимфатические узлы.
2. Радикальная вульвэктомия с пахово-бедренной лимфаденэктомией проводится после лучевой терапии на область вульвы у пациенток с большим первичным опухолевым поражением. Локальная адъювантная лучевая терапия СОД 45–50 Гр показана при стромальной инвазии опухоли более 5 мм, особенно если имеется метастатическое поражение лимфатических узлов. Облучение таза и паховых областей проводится, если метастатически изменены 2 и более паховых лимфатических узла.
3. Предоперационная лучевая терапия может проводиться в отдельных случаях для увеличения операбельности опухоли и для уменьшения размеров оперативного вмешательства. Эффективным является сочетание предоперационной лучевой терапии СОД до 55 Гр, разделенной на 2 курса с интервалом 2 нед, и химиотерапии, проводимой в начале каждого курса по схеме ;фторурацил ;(750 мг/м2, ежедневно, в течение 5 дней) и ;митомицин ;(15 мг/м2, однократно).
4. Для тех пациенток, которым невозможно проведение радикальной вульвэктомии из-за сопутствующих заболеваний или распространенности процесса, единственным методом лечения, который повысит выживаемость больных данной категории, может оказаться радикальная лучевая терапия. Когда планируется лучевая терапия как основной метод лечения рака вульвы, американские врачи предпочитают сочетать ее с химиотерапией по схеме ;фторурацил ;(1 г/м2, ежедневно, в течение 5 дней) или ;фторурацил ;(1 г/м2, ежедневно, в течение 5 дней) с ;цисплатином ;(100 мг/м2, в 1 день). Четыре курса химиотерапии и лучевая терапия приводят к полной регрессии в 53–89% случаев первично неоперабельной опухоли или тех случаев, когда необходима экзентеративная хирургия. СОД должна быть не менее 65 Гр.
Стадия IV рака вульвы
Наиболее трудной задачей для любого клинициста является лечение больных раком вульвы IVA-IVB стадий. Распространение опухоли на слизистую мочевого пузыря, верхней трети уретры или прямой кишки предполагает либо выполнение сверхрадикальных операций, либо сочетание химиолучевой терапии с паллиативными хирургическими вмешательствами. Отдаленные результаты лечения этой категории больных в течение длительного периода времени остаются неудовлетворительными и не превышают 10–20%.
Методы выбора
1. Радикальная вульвэктомия с тазовой экзентерацией.
2. Хирургическое лечение с предоперационной лучевой терапией при значительном местном распространении процесса. Локальная адъювантная лучевая терапия в дозе 45–50 Гр показана при стромальной инвазии опухоли более 5 мм, особенно если имеется метастатическое поражение лимфатических узлов. Облучение таза и паховых областей проводится, если метастатически изменены 2 и более паховых лимфатических узла.
3. Облучение больших первичных опухолей делает возможным проведение радикальной операции. Лучевая терапия в дозе 55 Гр с подключением ;фторурацила ;оказывается эффективна.
4. Для больных, которым отказано в проведении радикальной вульвэктомии по тем или иным показаниям, радикальная лучевая терапия является методом выбора и повышает выживаемость. Возможно присоединение химиотерапии ;фторурацилом ;или ;фторурацилом ;с ;цисплатином. Лучевые осложнения в виде позднего фиброза, атрофии, телангиэктазии и некроза могут быть минимизированы, если не давать полной чрезмерной дозы, а фракционировать лучевую нагрузку. Общая доза составляет 54–65 Гр.
Рецидивы рака вульвы
Не менее трудной задачей клинической онкогинекологии является лечение рецидивов рака вульвы, которые могут быть локальными, регионарными или локально-регионарными. Частота рецидивов рака вульвы зависит от стадии заболевания, глубины инвазии и, что наиболее важно, поражения регионарных лимфатических узлов. Частота рецидивов при плоскоклеточном раке вульвы составляет в среднем 15–40%. Прогноз при рецидиве рака вульвы, в первую очередь, зависит от локализации рецидива и сроков возникновения. Так, лечение эффективно только при изолированном рецидиве в области вульвы без поражения лимфатических узлов. Стойкое излечение при рецидивах в области вульвы наблюдается в 40–80%. При диагностировании локального рецидива через 2 года и более после проведения первичной операции комбинация лучевой терапии и оперативного лечения дает 5-летнюю выживаемость более 50%.
Причины возникновения рецидива:
— нерадикальная резекция опухоли (ближе 1 см от края опухоли — 50%),
— глубокая инвазия,
— большой размер опухоли.
Тактика лечения при рецидиве рака вульвы индивидуальна: если возможно, то выполняется радикальная резекция, в остальных случаях — комбинированное или комплексное лечение.
У больных с метастазами в паховые лимфатические узлы, особенно множественными, двусторонними, с прорастанием в окружающие ткани, велика вероятность возврата заболевания с поражением подвздошных или тазовых лимфатических узлов и внутренних органов. Прогноз для пациенток с регионарным или системным возвратом заболевания неблагоприятный. Метастазы в лимфатические узлы не позволяют выполнить радикальной резекции, лучевая терапия при больших рецидивах неэффективна, а эффективные схемы химиотерапии на сегодняшний день отсутствуют. Незначительному проценту больных с поражением подвздошных лимфатических узлов возможно проведение радикальной лимфаденэктомии с последующей лучевой терапией.
Методы выбора
1. Широкое локальное иссечение с/без лучевой терапии при локальных рецидивах.
2. Радикальная вульвэктомия и тазовая экзентерация.
3. Химиолучевое лечение с/без оперативного лечения.
4. Применение нестандартной химиотерапии или других видов системного лечения больным с метастатическими опухолями.
Профилактика
Несмотря на то что рак вульвы относится к визуально выявляемым заболеваниям, значительное число больных поступает на лечение при наличии распространенного процесса. С одной стороны, это связано с анатомическими особенностями наружных половых органов, имеющих обильно развитую кровеносную и лимфатическую сети и характеризующихся выраженной пролиферативной активностью плоскоклеточного рака и ранним метастазированием в регионарные зоны, с другой стороны — с отсутствием патогенетически обусловленной профилактики и эффективного лечения нейродистрофических процессов. Ведь данная категория больных — женщины пожилого и старческого возраста, которые длительное время не обращались к врачу и занимались самолечением. Другая причина связана с врачебными ошибками — больным длительно и необоснованно не выполняется биопсия опухоли и проводится противовоспалительное лечение. С этих позиций правильная оценка анамнеза, клинической симптоматики и рациональное построение диагностического процесса могут способствовать своевременному распознаванию рака этой локализации. По сводным данным FIGO, 5-летняя выживаемость больных раком вульвы I-III стадий составляет всего 47,3%. По данным Novak, адекватно проведенное лечение и хирургическое стадирование позволяют излечить 72% больных раком вульвы I-III стадий. До настоящего времени для большинства специализированных клиник мира приведенные результаты лечения рака вульвы труднодостижимы.
На сегодняшний день существуют 3 основных пути улучшения результатов лечения:
1. Первичная и вторичная профилактика.
2. Ранняя диагностика.
3. Адекватное лечение.
Согласно патогенетическим механизмам развития рака вульвы, ;первичная профилактика ;должна быть направлена на предупреждение заболеваний, передающихся половым путем, нормализацию обменно-эндокринных нарушений и т.д.
К мерам ;вторичной профилактики ;можно отнести своевременное и адекватное лечение фоновых нейродистрофических процессов и особенно внутриэпителиальной неоплазии вульвы.
Направления профилактики рака вульвы:
— лечение нейродистрофических процессов (плоскоклеточной гиперплазии и склерозирующего лишая) не должно начинаться без гистологического уточнения диагноза;
— при плоскоклеточной гиперплазии, возвышающейся над поверхностью кожи (гипертрофические и бородавчатые формы), предпочтение следует отдавать хирургическому лечению, криодеструкции или применению СО2-лазера;
— консервативное медикаментозное лечение нейродистрофических заболеваний при отсутствии эффекта не должно продолжаться более полугода. В этих случаях следует обсудить вопрос о хирургическом лечении;
— у больных нейродистрофическими заболеваниями при гистологическом исследовании с высокой частотой выявляются дисплазия и преинвазивный рак вульвы. Хирургическое лечение дисплазии и рака ;in situ ;— наиболее эффективный путь предупреждения инвазивного рака вульвы;
— расширение показаний для хирургического лечения при дисплазиях вульвы;
— разработка методик щадящих органосохраняющих операций и крио— или лазерной деструкции у больных молодого возраста с дисплазией или преинвазивным раком вульвы, что будет способствовать сексуальной реабилитации женщин.
Литература
FIGO (1989). Annual report on the results of treatment in gynecological cancer//Int. J. Gynecol. Obstet.— 1989.— V. 28.— P. 189–193.
FIGO (1990). Changes in gynecological cancer staging by the International Federation of Gynecology and Obstetrics//Am. J. Obstet. Gynecol.— 1990.— V. 162.— P. 610–611.
Binder S.W. et al. ...Gynecol. Oncology.— 1990.— V. 37 (1).— P. 9–16, UI:90215384.
Homesley H.D. et al. ...Am. J. Obstet. Gynecol.— 1991.— V. 164 (4).— P. 997–1004.
Boyce J. et al. ...Gynecol. Oncology.— 1985.— V. 20 (3).— P. 364–377.
Sedlis A. et al. ...Am. J. Obstet. Gynecol.— 1987.— V. 156 (5).— P. 1159–1164.
Binder S.W. et al. ...Gynecol. Oncology.— 1999.— V. 49 (3).— P. 279–283.
Homesley H.D. et al. ...Gynecol. Oncology.— 1993.— V. 49 (3).— P. 279–283.
Malfetano J.H. et. al. ...Journal of Surgical Oncology.— 1985.— V. 30 (2).— P. 124–131.
Stehman F.B. et al. ...Obstetrics and Gynecology.— 1992.— V. 79 (4).— P. 490–497.
Hacker N.F. et al. ...Cancer.— 1993.— V. 71 (4, suppl.).— P. 1673–1677.
Thomas G.M. et al. ...Gynecol. Oncology.— 1991.— V. 42 (1).— P. 9–21.
Hoffman M.S. et al. ...Obstet. and Gynecol. Survey.— 1989.— V. 44 (4).— P. 227–233.
Homesley H.D. et al. ...Am. J. Obstet. Gynecol.— 1991.— V. 164 (4).— P. 997–1004.
Homesley H.D. et al. ...Gynecol. Oncology.— 1993.— V. 49 (3).— P. 279–283.
Anderson J.M. et al. ...Int. J. Radiation Oncology, Biology, Physics.— 1995.— V. 32 (5).— P. 1351–1357.
Russell A.H. et al. ...Gynecol. Oncology.— 1992.— V. 47 (1).— P. 14–20.
Berek J.S. et al. ...Gynecol. Oncology.— 1991.— V. 42 (3).— P. 197–201.
Koh W.J. et al. ...Int. J. Radiation Oncology, Biology, Physics.— 1993.— V. 26 (5).— P. 809–816.
Описание проверено экспертом
Оцените статью:
- Рак вульвы
- Базальноклеточная карцинома вульвы
- Карцинома вульвы
Вирус папилломы человека: проблема, которая касается всех
Разрушаем миф: вирус папилломы человека может вызывать рак не только шейки матки, но и другие онкозаболевания у мужчин и женщин.
Опубликовано на сайте: 16.10.25 | Обновлено на сайте: 14.10.25
Полужирным шрифтом выделены лекарства, входящие в справочники текущего года. Рядом с названием препарата может быть указан ежегодный уровень индекса информационного спроса (показатель, который отражает степень интереса потребителей к информации о лекарстве).