C74 Злокачественное новообразование надпочечника, МКБ-10
Отредактировано: 02.04.2024
д.м.н. Баронин А.А.
ГУ РОНЦ им. Н.Н. Блохина РАМН
Классификация опухолей надпочечников. Опухоли коры надпочечников. Опухоли мозгового слоя надпочечников. Диагностика. Лечение
Первичные опухоли надпочечников относятся к одному из важных и трудных в диагностическом и лечебном плане разделов клинической онкологии. Эти заболевания объединяют группу различных вариантов опухолей, в число которых входят и гормонально-активные опухоли надпочечников.
Классификация опухолей надпочечников
Общепринято классифицировать опухоли надпочечников на ;доброкачественные и злокачественные. Это имеет важное практическое значение для прогноза заболевания, т.к. хирургическое удаление доброкачественной опухоли ведет к полному выздоровлению, тогда как прогноз при злокачественных новообразованиях неблагоприятный. При этом морфологические признаки злокачественности опухолей надпочечников дискутируются до настоящего времени.
Если до недавнего времени считалось, что опухоли надпочечников являются редкой патологией и составляют не более 0,6% всех злокачественных опухолей (Дорохов И.И., Непомнящая К.В., 1978; Казеев К.Н., 1974; Поршин К.К., Кудрявцев В.Н., 1987; Рыбаков С.И., 1990), то в настоящее время благодаря широкому внедрению в повседневную клиническую практику таких неинвазивных и информативных методов диагностики, как УЗИ, КТ, МРТ резко возросло число обнаруживаемых новообразований в забрюшинном пространстве. Часть их локализуется в надпочечнике, и в большинстве случаев эти новообразования являются опухолями, исходящими либо из коркового, либо мозгового его слоев (Бронштейн М.Э., Кузнецов Н.С., 1998; Мамаева В.Г.; Kohler R. et al., 1976; Lack T.T., et al, 1990; Neville A.M. et al., 1995).
Надпочечники имеют сложное гистологическое строение и состоят из двух отличающихся друг от друга в эмбриологическом и морфологическом отношениях слоев: коркового и мозгового (Зографски Ст., 1977).
Кора надпочечников развивается из мезодермальной ткани. Корковый слой состоит из трех зон: клубочковой, пучковой и сетчатой и образован железистой и соединительной тканью. Клубочковая зона — самый поверхностный слой, который вырабатывает минералкортикоиды, регулирующие внутри- и внеклеточную концентрацию натрия и калия. Пучковая зона (самая широкая) продуцирует 70% гормонов коры. Основными их представителями являются кортизон, гидрокортизон и кортикостерон, которые регулируют углеводный, белковый и жировой обмен. В сетчатой зоне синтезируются половые гормоны — андрогенкортикоиды, эстрогенкортикоиды, которые определяют вторичные половые признаки.
Мозговой слой содержит хромаффинные клетки, которые окрашиваются хромовыми солями, и симпатические нервные клетки. Мозговое вещество синтезирует катехоламины. Следует иметь в виду развитие катехоламинсекретирующих опухолей из нехромаффинных клеток симпато-адреналовой системы. Возможность такого их происхождения объясняется общностью эмбриогенеза феохромоцитов и других клеток нервной ткани. ;Феохромоцитомы ;развиваются из двух эмбриональных зачатков — нервной трубки и ее гребешка, где стволовые клетки (симпатогонии) дифференцируются на симпатобласты и хромаффиннобласты. Обе популяции клеток в процессе эмбриогенеза в последующем подвергаются дальнейшей дифференциации. Именно этим и объясняется разнообразие гистологической структуры феохромоцитом. Опухоли, исходящие из мозгового слоя надпочечников, могут состоять из феохромоцитомы и нейробластомы, ганглионейробластомы или ганглионевромы. Преобладающим компонентом в таких сложных опухолях чаще всего является феохромоцитома. Нередки случаи переходного строения — от феохромоцитомы к нейробластоме. Наряду с такого рода опухолями встречаются опухоли чисто нейрогенного гистогенеза: ганглиомы, ганглионевромы, нейрофибромы (Travis W.D. et al., 1990). Эти опухоли, как правило, доброкачественные, имеют строение соответствующих опухолей другой локализации. Крайне редко в надпочечниках могут встречаться ;гемангиомы, ангиосаркомы, лимфангиомы, лейомиомы и лейомиосаркомы, лимфомы, опухоли стромы гонадального тяжа, первичные меланомы. ;Они также не отличаются по структуре от соответствующих опухолей типичной локализации (Travis W.D. et al., 1990).
Среди объемных образований надпочечников, протекающих без эндокринных нарушений, встречаются миелолипомы (Medeiros L.J. et al., 1992). Это доброкачественные образования, состоящие из зрелой жировой соединительной ткани и гемопоэтических элементов. Они нередко сочетаются с гормонально-активными и “немыми” опухолями надпочечников. Достигая больших размеров, могут вызывать атрофические изменения в надпочечнике и приводить к развитию гипокортицизма. Нередко локализуются и вне надпочечника: в периренальной и периадреналовой клетчатке. Не всегда инкапсулированы (Бронштейн М.Э., Кузнецов Н.С., 1998). Патогенез и клиническая картина гормонально-активных опухолей коры надпочечников обусловлены гиперпродукцией тех или иных стероидных гормонов, в зависимости от структуры опухоли. Нередко наблюдается картина смешанного гиперкортицизма, когда новообразование продуцирует несколько гормонов, различных по своему биологическому действию на организм.
Опухоли коры надпочечников
Гормонально-активные опухоли коры надпочечников
Альдостерома ;— опухоль, продуцирующая альдостерон, вызывает первичный альдостеронизм. ;Первичный альдостеронизм (синдром Конна) ;характеризуется определенным симптомокомплексом: гипертензией, мышечной слабостью и алкалозом с гипокалиемией. Морфологическим субстратом первичного альдостеронизма является опухоль, реже — гиперплазия коркового вещества надпочечников. По данным J. Conn (1955, 1964), одиночные аденомы (альдостеромы) встречаются у 70–90% больных, множественные — у 10–15%, гиперплазия коры надпочечников — у 9%. В целом опухолевые поражения надпочечников как причина первичного гиперальдостеронизма наблюдаются в 84% случаев, причем у 2–6% больных они носят злокачественный характер (Хирургия надпочечников, 2000).
Клинически ;синдром Конна ;отличается гипертензией (систолической и диастолической), умеренной полиурией и более или менее выраженным ослаблением отдельных мышечных групп.
Почти у всех больных отмечаются (могут быть положительными) симптомы Труссо и Хвостека. Слабость отдельных мышечных групп может переходить в скоропроходящие парезы, вызванные гипокалиемией. Эти симптомы сопровождаются усиленным аппетитом, чувством сухости во рту, головными болями.
При лабораторных исследованиях может отмечаться повышенное выделение альдостерона с мочой. Для диагностики гиперальдостеронизма применяется спиронолактоновый тест. При пробе с ;гидрохлоротиазидом ;уровень калия в крови при отсутствии гиперальдостеронизма и у больных с вторичным гиперальдостеронизмом существенно не меняется; у больных же с первичным альдостеронизмом — резко снижается.
Низкий уровень калия сопровождается электрокардиографическими изменениями. Алкалоз является характерным признаком синдрома.
Кортикостерома ;(глюкостерома) выделяет глюкокортикоиды и клинически проявляется синдромом Иценко — Кушинга. Различают 3 разновидности эндогенного синдрома Иценко — Кушинга:
1. ;Гипофизарный синдром Кушинга ;(болезнь Кушинга) обусловлен нерегулируемой избыточной секрецией АКТГ в аденогипофизе. Избыток АКТГ стимулирует продукцию глюкокортикоидов в коре надпочечников, что приводит к гиперкортизолемии.
2. ;Надпочечниковый синдром Иценко — Кушинга ;обусловлен нерегулируемой избыточной секрецией кортизола опухолями коры надпочечника или гиперпластической тканью коры надпочечников (узловая, реже — мелкоузелковая гиперплазия). При надпочечниковом синдроме Иценко — Кушинга уровень АКТГ в плазме понижен.
3. ;Эктопический синдром Иценко — Кушинга ;обусловлен нерегулируемой избыточной секрецией АКТГ негипофизарными злокачественными новообразованиями и характеризуется сильным повышением АКТГ в плазме.
Синдром Иценко — Кушинга имеет целый ряд характерных симптомов, таких как ожирение с распространением излишка жира, прежде всего, на теле, круглая форма лица (“лунообразное лицо”), истончение кожи и атрофия эластических волокон, в результате чего на животе, бедрах и ягодицах возникают красноватые дермоэктазии, мышцы ослабевают, появляется остеопороз, склеротические изменения в сосудах, сопровождающиеся гипертензией, стероидный диабет, протекающий с чрезмерным аппетитом и полиурией, наконец, алкалоз с низким уровнем калия и хлора в крови.
Вместе с чрезмерной секрецией кортизола увеличивается образование 17-кетостероидов с андрогенным влиянием. В результате появляются такие симптомы, как чрезмерное оволосение, глухой голос, акне, задержка менструаций, гипертрофия клитора. Гипертензия, низкий уровень калия, увеличенный уровень натрия являются результатами усиленной продукции альдостерона.
У всех больных, у которых имеет место ожирение вместе с гипертензией, расстройствами углеводного обмена, кожные дермоэктазии и остеопороз, следует исключить синдром Иценко — Кушинга.
При обычных исследованиях удается выявить нейтрофилию с лимфоцитопенией и эозинофилией, повышенный уровень сахара, гипокалиемию, гипохлоремию.
При определении гормональной активности коры надпочечников целесообразно проведение короткой пробы с ;дексаметазоном ;— повышение концентрации кортизола в сыворотке крови свидетельствует о гиперкортизолемии. Высокий уровень экскреции кортикостероидов с мочой также подтверждает диагноз синдром Иценко — Кушинга.
С целью дифференциальной диагностики гипофизарного и надпочечникового синдрома Иценко-Кушинга целесообразно проведение длинной пробы с ;дексаметазоном, при которой кортизол снижается более чем на 50% по сравнению с исходным уровнем при гипофизарном синдроме. При гипофизарном синдроме стимуляционная проба с кортиколиберином повышает почти на 90% уровни АКТГ и кортизола. У больных с эктопическим и надпочечниковым синдромом секреторной реакции на кортиколиберин нет.
Андростерома ;— опухоль, секретирующая преимущественно андрогены. Андростерома — гормонально-активная, вирилизирущая опухоль, продуцирующая мужские половые гормоны. Обычно она локализуется в эктопически расположенной надпочечниковой ткани (яичниках, широкой связке матки). Андростеромы относятся к редкой патологии (1–3% всех опухолей). Почти в 60% случаев андростерома бывает злокачественной, метастазирует в печень, легкие, забрюшинные лимфатические узлы. Андростерома чаще развивается у женщин, в основном до 35–40 лет. Отмечается особенно высокий процент злокачественных опухолей в детском возрасте, причем у девочек опухоль наблюдается в 5 раз чаще, чем у мальчиков.
Клинические проявления ;обусловлены вирилизирующими и анаболическими свойствами андрогенов. Степень вирилизации зависит от гормональной активности опухоли, длительности заболевания. У девочек раннего возраста заболевание характеризуется явлениями интерсексуализма и преждевременным физическим развитием: наблюдается гипертрихоз, увеличение клитора, низкий, грубый голос, угри на лице и туловище.
Под влиянием анаболического эффекта андрогенов усиливается развитие мышц, ускоряются процессы роста одновременно с ранним закрытием эпифизарных зон роста. Характерны низкорослость с непропорциональным укорочением конечностей и хорошо развитыми мышцами, развитие вторичных половых признаков по гетеросексуальному типу. Преждевременное половое развитие нельзя считать истинным, поскольку оно, как правило, выражается появлением вторичных половых признаков, в то же время половые железы соответствуют возрасту ребенка. По мере увеличения сроков заболевания становится более выраженным мужское телосложение, женские черты сглаживаются, уменьшается подкожно-жировой слой, выделяется мускулатура и увеличивается ее масса. Молочные железы подвергаются более или менее выраженной атрофии.
Менструации либо вообще не появляются, либо нарушаются по типу олигоменореи, и вскоре наступает аменорея. У женщин начинают расти борода и усы, голова начинает лысеть. Самочувствие больных на ранних стадиях остается удовлетворительным. Под воздействием андрогенов могут возрасти физическая активность и работоспособность.
У мальчиков развитие андростеромы сопровождается преждевременным половым развитием. Половой член значительно увеличивается, но семенники остаются недоразвитыми. Хорошо выражены вторичные половые признаки, рано появляется половое влечение.
У больных андростеромой не выявляется значительных обменных нарушений. Количество андрогенов, определяемых в крови и в моче, возрастает в десятки раз.
Кортикоэстерома ;— опухоль, выделяющая эстрогены. Встречается крайне редко. Эстрогено-генитальный синдром наблюдается главным образом у молодых мужчин. Больные жалуются на общую слабость, увеличение грудных желез, ожирение, выпадение волос на лице, половую слабость. Не всегда перечисленные симптомы встречаются одновременно. Наиболее частым признаком кортикоэстеромы является гинекомастия.
Cмешанные опухоли. “Чистые” опухоли типа альдостером, кортикостером, андростером, кортикостером встречаются редко. Чаще обнаруживаются смешанные опухоли с преобладанием признаков того или иного синдрома в зависимости от повышенного образования тех или иных стероидов. Такие опухоли, как правило, имеют смешанное гистологическое строение.
Гормонально-неактивные опухоли коры надпочечников
Гормонально-неактивные опухоли коры надпочечников протекают обычно без клинических и биохимических признаков нарушения функции соответствующих слоев коры надпочечника; обнаруживаются в любом возрасте у лиц обоего пола в 0,5–10% случаев, нередко выявляются при обследовании по поводу другого заболевания. Для обозначения подобных опухолей наиболее часто используется термин "инциденталома“ (от англ. incidental — случайный).
Среди гормонально-неактивных опухолей коры надпочечников основную массу составляют аденомы — светлоклеточные (преобладающий вариант), смешанно-клеточные (из светлых и темных клеток) и темноклеточные (наиболее редкий вариант). Аденомы составляют 30% и более от числа всех гормонально-неактивных опухолей (Bvans H.L., 1996).
Адренокортикальные раки встречаются значительно реже аденом (примерно в 4 раза), составляя, по данным различных авторов, не более десятых или даже сотых долей процента от числа всех опухолей надпочечников (Van Slooten H. et al., 1985).
Опухоли мозгового слоя надпочечников
Опухоли мозгового слоя надпочечников (феохромоцитомы) являются опухолями нейроэктодермального происхождения из хромаффинных клеток, продуцирующих катехоламины (адреналин, норадреналин, дофамин).
Наиболее компактное их расположение наблюдается в мозговом слое надпочечников, хотя они могут встречаться по обе стороны аорты в месте отхождения нижней брыжеечной артерии (орган Цуккеркандля), в симпатических парааотральных ганглиях, стенке мочевого пузыря, в воротах печени и почек (Калинин А.П. и др., 1998). Феохромоцитомы чаще развиваются в возрасте 20–50 лет. Сведения о преимущественной заболеваемости мужчин или женщин отсутствуют. По литературным данным (Мокроусов Б.М.и др., 1986), до 80% опухолей мозгового слоя надпочечников располагаются в одном из надпочечников, в 10% бывают множественными и в 10% — локализуются вне надпочечников. Возможны злокачественные варианты ;феохромоцитом ;с метастазированием.
По клиническому течению различают несколько форм феохромоцитом: бессимптомную феохромоцитому, симпато-адреналовую феохромоцитому с пароксизмальной гипертензией и симпато-адреналовую феохромоцитому с постоянной гипертензией (Travis W.D. et al., 1990). В отдельную группу (1–2% случаев) выделяются нефункционирующие опухоли хромафинной ткани, обнаруживаемые случайно при обследовании по поводу другого заболевания (Mena A. et al., 1997).
Наиболее известна классическая — ;пароксизмальная ;форма, при которой появляются гипертонические кризы. В межкризовые периоды АД остается нормальным. Внезапное повышение АД может сопровождаться побледнением или покраснением кожных покровов, чувством страха, сердцебиением, парестезиями. Зрачки после кратковременного расширения резко суживаются, нарушается зрение. Отмечается набухание вен шеи, судороги, резкая потливость, озноб, повышение температуры тела. Нередко появляются одышка, боли в животе, поясничной области, за грудиной. Длительность приступов может длиться от нескольких минут до нескольких часов с исходом в улучшении самочувствия, иногда с элементами эйфории, потливостью, полиурией.
Важными диагностическими признаками катехоламинового криза являются лейкоцитоз, гипергликемия и глюкозурия. В межкризовый период у части больных выявляется нарушение толерантности к углеводам (Казеев К.Н., 1966).
Постоянная форма ;артериальной гипертензии характеризуется стойким повышением АД без кризов и напоминает течение гипертонической болезни, от которой ее бывает трудно отличить. Нередко лишь отсутствие эффективности традиционной гипотензивной терапии наводит на мысль о возможности надпочечникового происхождения стойкой гипертензии (Керцман Г.И., 1974).
Cмешанная форма ;отличается тем, что гипертонические кризы возникают на фоне постоянно повышенного АД, протекают менее типично, чем у больных с ;пароксизмальной формой ;— чаще доминируют симптомы хронического поражения сердечно-сосудистой системы (Калинин А.П. и др., 1998).
Злокачественные опухоли надпочечников характеризуются не только степенью своей гормональной активности, но и особенностями метастазирования. Для них характерны как лимфогенный, так и гематогенный путь метастазирования.
Злокачественные опухоли коркового слоя надпочечников обладают выраженной тенденцией к преимущественному гематогенному метастазированию, что объясняется особой подвижностью клеток мезенхимального генеза вообще, обилием тонкостенных сосудов в строме опухоли, а также иммунодепрессантным эффектом глюкокортикоидов, освобождающихся при некрозах и кровоизлияниях в опухоли. Гематогенные метастазы отмечаются в легких, костной системе, головном мозге, ЖКТ, почках, печени, матке, железах внутренней секреции (Дорохов И.И., Непомнящая К.В., 1978).
Злокачественные опухоли хромафинной ткани надпочечников также характеризуются быстрым распространением метастазов в легкие, кости, головной мозг, лимфатические узлы.
Лимфатический отток от надпочечников происходит в разных направлениях. От верхних полюсов надпочечников отводящие лимфатические сосуды сопровождают верхнюю надпочечниковую и нижнюю диафрагмальную артерии. Они проникают через диафрагму и впадают в задние средостенные лимфатические узлы, располагающиеся на уровне ThIX-X. Регионарными лимфатическими узлами для обоих надпочечников являются лимфатические узлы, локализующиеся позади аорты на уровне ThXI-XII.
Регионарные лимфатические узлы левого надпочечника располагаются на уровне отхождения от аорты почечных, надпочечниковых артерий и артерий яичка (яичника). Левые латероаортальные и преаортальные лимфатические узлы обычно располагаются в промежутке между отхождением от аорты верхней и нижней брыжеечных артерий.
Регионарные лимфатические узлы правого надпочечника располагаются впереди аорты, между аортой и нижней полой веной, позади нижней полой вены и справа от аорты, чаще всего — на уровне отхождения от аорты почечных и надпочечниковых артерий, но могут также находиться у корня нижней и верхней брыжеечных артерий (Блинова Л.И., 1971).
Диагностика
Диагностика ;гормонально-активных опухолей надпочечников ;при наличии соответствующих клинических симптомов заключается в топической диагностике новообразования, определении степени распространенности, подтверждении диагноза исследованием гормонального статуса и проведением соответствующих проб.
Значительно сложнее диагностика ;гормонально-неактивных опухолей, когда отсутствуют специфические клинические проявления поражения надпочечников, а гормональный статус не изменен.
Задача начального этапа обследования больного, основанного на жалобах, данных физикального и гормонального исследований, — не столько постановка правильного диагноза, сколько необходимость заподозрить у больного наличие опухоли надпочечника.
Осмотр больного и пальпация должны проводиться, как и при подозрении на любое онкологическое заболевание, тщательно и всесторонне. Отсутствие при пальпации опухоли в правом или левом подреберьях не исключает необходимости дальнейшего осмотра всех органов. Обнаружив опухоль, необходимо определить ее подвижность, размеры, консистенцию.
Следующим этапом в обследовании больного с подозрением на опухоль надпочечника является установление наличия и локализации опухоли. Основными задачами, стоящими перед специальными методами топической диагностики, являются, с одной стороны, установление диагноза в максимально сжатые сроки, а с другой — оценка распространенности опухолевого процесса для определения возможности и объема предполагаемого оперативного вмешательства.
Важное место среди инструментальных методов исследования опухолей надпочечников в настоящее время занимает УЗИ (рис. 1). Это, в первую очередь, обусловлено простотой его выполнения, высокой достоверностью полученных результатов, а также быстротой и доступностью его выполнения (Демидов В.Н. и др., 1991). По мнению большинства авторов, УЗИ позволяет выявить опухоли надпочечников при минимальном диаметре от 1 до 2 см (Gunhter R.W., 1984; Zografos G.C. et al., 1994).
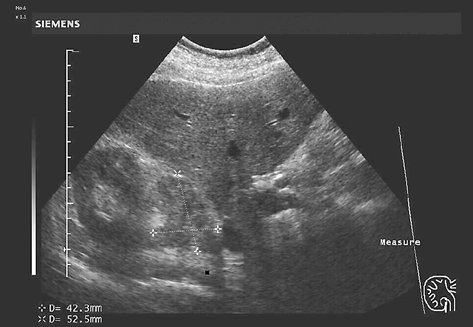
Рисунок 1. УЗИ — опухоль правого надпочечника
Значительно улучшает качество диагностики опухолей надпочечников использование КТ. Минимальная величина опухоли, определяемая этим методом, составляет от 0,5 до 1 см (Бондаренко В.О., 1986). КТ позволяет определить топографию надпочечников, форму, величину, структуру. Точность КТ в диагностике опухолей надпочечников в настоящее время составляет 80–95,7% (Авдеева Т.Ф. и др., 1992) (рис. 2).
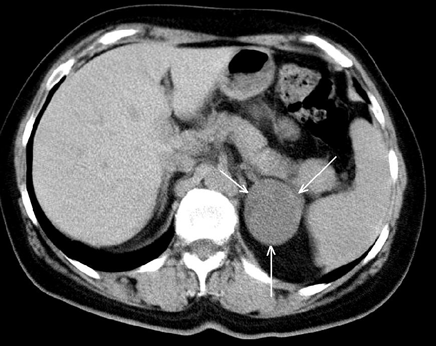
Рисунок 2. КТ — опухоль (аденома) левого надпочечника
Наряду с преимуществами КТ имеет и ряд недостатков. При больших размерах опухоли трудно определить ее исходную локализацию, распространенность на другие органы и магистральные сосуды (Григорян С.В. и др., 1986). Основным методом, позволяющим ответить на данные вопросы, является АГ. Но, несмотря на тридцатилетний опыт применения АГ при опухолях надпочечников, до настоящего времени не установлено специфических ангиографических признаков, присущих какой-либо определенной гистологической форме опухоли. Тем не менее ангиографическая картина в большинстве случаев достаточно характерна, чтобы установить исходную локализацию опухоли, степень ее васкуляризации, источники кровоснабжения и распространение на окружающие органы и ткани (рис. 3, 4).
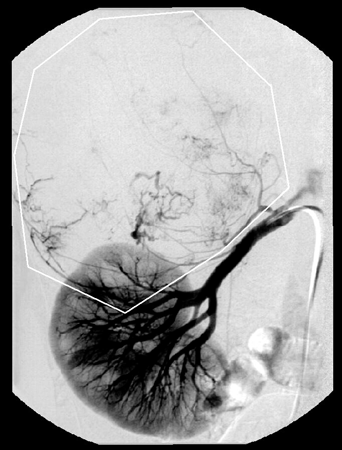
Рисунок 3. Селективная артериография (артериальная фаза) — умеренно васкуляризированная опухоль (феохромоцитома) правого надпочечника
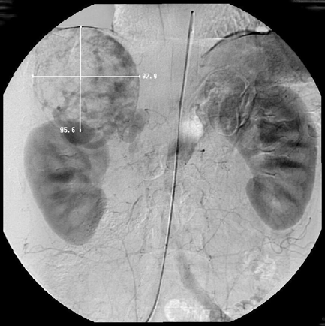
Рисунок 4. Ангиография (паренхиматозная фаза) — умеренно васкуляризированная опухоль (феохромоцитома) правого надпочечника
По данным различных авторов, точность ангиографической диагностики опухолей надпочечников составляет 78–95% (Kohler R. et al., 1976; Zografos G.C. et al., 1994). При правосторонней локализации опухоли, особенно больших размеров, для выявления взаимосвязи с нижней полой веной необходимо выполнение нижней каваграфии, желательно в двух проекциях (рис. 5, 6).
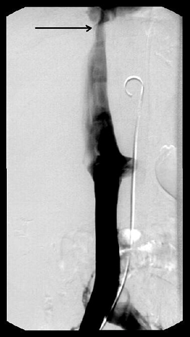
Рисунок 5. Нижняя каваграфия (прямая проекция) — сужение и сдавление нижней полой вены опухолью правого надпочечника
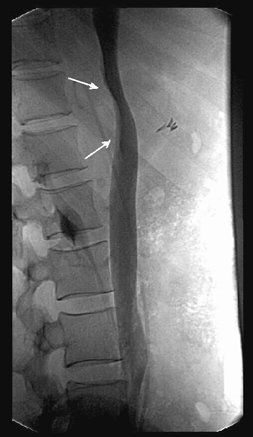
Рисунок 6. Нижняя каваграфия (боковая проекция) — оттеснение кпереди и сужение нижней полой вены опухолью правого надпочечника
С начала 80-х гг. XX в. в клинической практике появился принципиально новый метод диагностики — МРТ, основанная на явлении ядерно-магнитного резонанса (рис. 7, 8, 9).
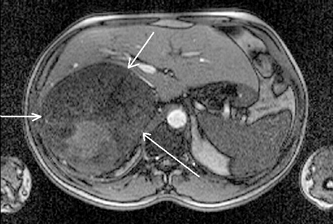
Рисунок 7. МРТ (горизонтальная проекция) — опухоль правого надпочечника
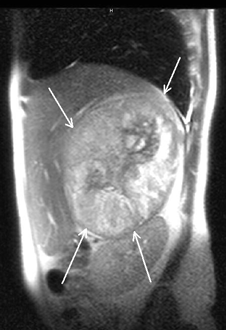
Рисунок 8. МРТ (сагиттальная проекция) — опухоль правого надпочечника
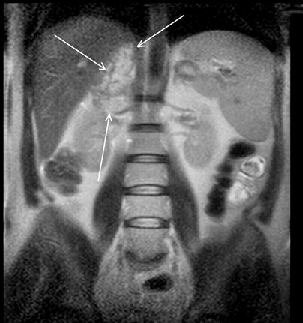
Рисунок 9. МРТ (фронтальная проекция) — опухоль правого надпочечника
Основные достоинства МРТ — неинвазивность, безвредность, трехмерный характер получения изображений. Однако этот метод является одним из самых дорогостоящих, и о применении МРТ при опухолях надпочечников существуют разноречивые мнения. По мнению Nakao Y.et al. (1993), МРТ перспективна для выявления опухолей малых размеров, а Н. Лавин (Эндокринология, 1999) считает, что МРТ в некоторых случаях дополняет результаты КТ, но при малых размерах опухоли надпочечника чувствительность этого метода не превышает чувствительности КТ. Однако, несмотря на использование различных инструментальных методов, точный диагноз, особенно при ;гормонально-неактивных опухолях, позволяет установить лишь морфологическое исследование, которое возможно при исследовании материала, полученного при аспирационной тонкоигольной биопсии под контролем УЗИ или КТ (Giron J., 1997; Petronio R., 1985) (рис. 10). Точность метода равняется 80–90% (Gonczi I. et al., 1987).
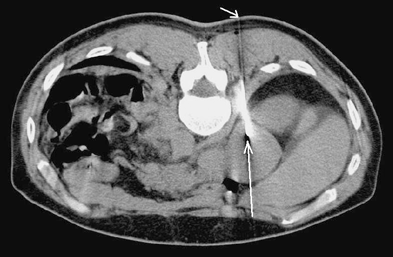
Рисунок 10. Тонкоигольная пункция опухоли (адренокортикальный рак) левого надпочечника под контролем КТ
Однако при гормонально-активных опухолях выполнение биопсии чревато развитием криза (Хитрова А.Н., 1996).
Лечение
Основным методом лечения опухолей надпочечников в настоящее время является хирургический.
Хирургическое лечение
Само наличие опухоли надпочечников уже служит показанием к оперативному лечению. Ни сопутствующие заболевания, ни большие размеры опухоли не являются абсолютными противопоказаниями к операции.
Противопоказаниям могут быть тяжелые сопутствующие заболевания, при которых противопоказано любое оперативное вмешательство; опухоли с множественными отдаленными метастазами.
Оперативные вмешательства при опухолях надпочечников относятся к категории довольно сложных. Это обусловлено глубиной расположения этого органа, сложными анатомическими взаимоотношениями с окружающими органами, опасностью повреждения крупных сосудов и близлежащих органов. Поэтому выбор оптимального операционного доступа к надпочечникам должен удовлетворять следующие требования: быть малотравматичным, создавать наибольший простор в ране, обеспечивая хорошую видимость, давать возможность для широкой ревизии органов брюшной полости и путей метастазирования (Клименков А.А., Сельчук В.Ю., Неред С.Н. и др., 1998). Выбор операционного доступа зависит от размеров опухоли, ее гормональной активности, локализации.
В настоящее время описано большое количество различных хирургических доступов к надпочечникам. Принципиально их можно разделить на 4 группы: чрезбрюшинные, трансторакальные, экстраперитониальные и комбинированные. Каждый из них имеет свои преимущества и недостатки, поэтому строго определенных показаний к выбору того или иного доступа до настоящего времени нет.
Чрезбрюшинные доступы ;(срединная, пара- или трансректальная лапаротомия) имеют преимущества при неуточненной локализации ;феохромоцитомы ;и адрено-кортикального рака c явлениями синдрома Иценко — Кушинга, т.к. позволяют провести ревизию не только обоих надпочечников, но и забрюшинного пространства, яичников, матки и других мест редкой локализации гормонально-активных опухолей. Из этих доступов достаточно просто выполнить лимфодиссекцию в аорто-кавальном промежутке. Недостатком этих доступов, особенно у тучных больных, является большая глубина операционного поля, что нередко требует мобилизации двенадцатиперстной кишки справа и мобилизации селезеночного изгиба ободочной кишки слева, не позволяя без технических трудностей выполнить удаление надпочечника с опухолью и эффективно бороться с массивными кровотечениями из нижней полой вены при ее повреждениях.
Преимуществом поперечных или подреберных абдоминальных доступов является обеспечение лучших условий для визуализации обоих надпочечников, при этом ревизия органов брюшной полости и значительной части забрюшинного пространства осуществляется проще, чем при срединной лапаротомии. К недостаткам этих доступов следует отнести большую травматизацию из-за нарушения целостности прямых мышц живота.
К достоинствам ;внебрюшинных доступов, иногда с резекцией XII ребра, относятся: относительная техническая простота, отсутствие в пределах операционной раны жизненно важных органов, сохранение целостности брюшины и плевры. Однако значительная глубина узкой раны не всегда позволяет создать широкий обзор забрюшинного пространства, затрудняет удаление надпочечника. Кроме того, подобные доступы не позволяют провести ревизию контралатерального надпочечника и, в случае необходимости, выполнить лимфодиссекцию. Исходя из вышеизложенного, в онкологии поясничные доступы нашли ограниченное применение.
Довольно широко используется комбинированный ;абдоминоторакофренотомический доступ, который является удобным для удаления опухоли любой односторонней локализации. При этом хирургическом доступе создаются оптимальные условия оперирования с широким обзором удаляемой опухоли, окружающих ее органов и магистральных сосудов. Особенно важно его применение при вовлечении в опухолевый процесс нижней полой вены, как правило, ее боковой или задней стенок, т.к. резекцию или ушивание стенки нижней полой вены наиболее легко осуществить именно из этого разреза. Этот доступ является и наиболее физиологичным, т.к. разрез в X межреберье без пересечения ребер вызывает небольшую травму сосудов, нервов, мышц.
В конце 80-х — начале 90-х гг. ХХ в. в литературе появились публикации о применении нового метода удаления надпочечников — ;лапароскопической адреналэктомии. Описано несколько видов эндовидеохирургических доступов к надпочечникам: ;трансабдоминальный, ретроперитониальный, трансторакальный. Наибольшее распространение получила ;лапароскопическая адреналэктомия. Преимуществами ;лапароскопической адреналэктомии ;являются: небольшое количество интраоперационных осложнений, незначительный болевой синдром, малая травматичность, сокращение пребывания пациента в стационаре, быстрое восстановление работоспособности. Однако до настоящего времени нет единого мнения о показаниях к ;лапароскопической адреналэктомии. При этом большинство хирургов (Fernandes-Cruz L., 1966; Henry J.F. et al., 1996) считают, что при злокачественных опухолях и при размерах опухоли более 8 см лапароскопические вмешательства применять не следует.
Успех хирургического лечения опухолей надпочечников во многом зависит от предоперационной подготовки, адекватности обезболивания, правильности ведения послеоперационного периода.
Предоперационная подготовка должна проводиться с учетом степени гормональной активности опухоли, проявлений заболевания, его осложнений и сопутствующей патологии. Нередко она может продолжаться несколько недель и требует совместных усилий терапевта-эндокринолога, хирурга и анестезиолога-реаниматолога. В целом подготовка заключается в коррекции метаболических нарушений, лечении сопутствующих заболеваний, санации очагов инфекции.
На любом этапе операции могут возникнуть опасные для жизни осложнения, но наиболее важными этапами являются непосредственные манипуляции с опухолью, поэтому требуется четкая организация проведения наблюдения за основными жизненными органами и системами. Обязательными условиями являются: кардиомониторирование на всех этапах операции, динамический контроль АД и ЦВД.
В раннем послеоперационном периоде больные нуждаются в интенсивном наблюдении и рациональной терапии стероидными гормонами, коррекции электролитного обмена, щелочных резервов крови. Наряду с профилактикой и лечением надпочечниковой недостаточности, необходимо учитывать тяжелое соматическое состояние больных. Расстройства минерального обмена, проявляющиеся чаще всего гипокалиемией, следует компенсировать введением препаратов калия в сочетании с антагонистами альдостерона (спиронолактон). Необходимы постоянный контроль уровня гликемии, достаточное введение жидкости, щелочных растворов, средств, улучшающих метаболизм и сократительную способность миокарда.
Химиолучевое лечение
В последние годы в литературе появились отдельные сообщения о химиолучевом лечении злокачественных опухолей надпочечников. Как правило, его применяют при первично-распространенных опухолях, либо при появлении метастазов после удаления первичной опухоли.
При опухолях коры надпочечников традиционна схема BEP: ;блеомицин ;— 30 мг, в/в, 1 раз в неделю, 9 недель; ;этопозид ;— 100 мг/м2, в 1–5 дни; ;цисплатин ;— 20 мг/м2, в 1–5 дни. ;Цисплатин ;и ;этопозид ;повторяют каждые 3 нед.
Для подавления секреции кортикостероидов при синдроме Иценко — Кушинга наибольшее применение находит ;митотан, который может применяться в сочетании с операцией или без нее, при иноперабельных опухолях коры надпочечника (кортикостеромах), сопровождающихся усиленным образованием кортикостероидов, а также после хирургического удаления кортикостером при повышенном уровне глюкокортикоидов в организме. Назначают препарат внутрь, начиная с 2–3 г/сут в первые 2–3 дня, затем из расчета 0,1 г/кг/сут. Суточную дозу дают в 3 приема, через 15–20 мин после еды. Лечение должно проводиться под контролем содержания кортикостероидов в крови и моче; определения производят 1 раз в 10–14 дней. Средняя курсовая доза 200–300 г. После приема каждых 80–100 г допускается перерыв 2–3 дня. Общая доза на курс и длительность терапии уточняются в процессе лечения в зависимости от эффективности. При применении ;митотана ;возможны: тошнота, понижение аппетита, головная боль, сонливость. Для улучшения переносимости рекомендуется прием витаминов.
При наличии неоперабельной злокачественной опухоли мозгового слоя надпочечника, рецидива опухоли и метастазов чаще всего применяется схема DOC: ;дакарбазин ;по 250 мг/м2, в/в, в 1–5 дни; ;винкристин ;по 1,5 мг/м2, в 5 день; ;циклофосфамид ;по 750 мг/м2, в/в, в 1 день. Циклы повторяют каждые 3 нед.
В литературе имеются весьма немногочисленные сообщения о применении лучевого лечения. Однако они касаются лишь использования лучевой терапии при наличии метастазов для уменьшения болевого синдрома.
Литература
Авдеева Т.Ф. и др. Возможности неинвазивных методов исследования в топической диагностике гормонально-активных опухолей надпочечников/Хирургия надпочечников. Материалы I Всесоюзного симпозиума, 1–3 июля 1992 г., Санкт-Петербург.- СПб., 1992.
Бирюкова М.С. Эндокринные заболевания и синдромы. Вирилизм. М.: Знание, 2000. — 165 с.
Блинова Л.И. Лимфатическая и кровеносная система надпочечников человека в возрастном аспекте: Автореф. ... дис. канд. мед. наук.- Иваново, 1971.- 24 с.
Бондаренко В.О. ...Применение ультразвука и новых видов энергии в диагностике, терапии и хирургии/Сб. науч. трудов под ред. А.И. Шатихина и др.- М., 1986.- С. 13–15.
Бронштейн М.Э. и др. Морфологические варианты “немых” объемных образований забрюшинного пространства/Современные аспекты хирургической эндокринологии. Материалы VII (IX) Всероссийского симпозиума по хирургической эндокринологии.- Липецк, 1998.- С. 31–33.
Григорян С.В. и др. ...Терап. архив.- 1989.- № 1.- C. 124–128.
Демидов В.Н. и др. Эхография надпочечников/Тезисы докладов I съезда ассоциации специалистов ультразвуковой диагностики в медицине.- М., 1991.
Дорохов И.И. и др. ...Вопр. онкологии.- 1978.- Т. 24.- № 1.- С. 42–48.
Зографски Ст. Эндокринная хирургия.- Cофия, 1977.- 594 с.
Казеев К.Н. Клиника, диагностика и хирургическое лечение опухолей хромафиннной ткани — феохромоцитом: Автореф. ... дис. канд. мед. наук.- М., 1966.- 13 с.
Казеев К.Н. Доброкачественные и злокачественные катехоламинпродуцирующие опухоли хромафинной ткани: Автореф. ... дис. докт. мед. наук.- М, 1974.
Калинин А.П. и др. Надпочечниковые и вненадпочечниковые феохромоцитомы.- М.: Нексил, 1998.- 36 с.
Керцман Г.И. Некоторые показатели изменений сердечно-сосудистой системы у больных феохромоцитомой: Автореф. ... дис. канд. мед. наук.- М., 1974.- 19 с.
Клименков А.А. и др. ...Вопр. онкологии.- 1998.- Т. 44.- № 5.- С. 541–546.
Мамаева В.Г. Инциденталомы надпочечников: клиника, диагностика, ведение больных: Автореф. ... дис. канд. мед. наук.
Мокроусов Б.М. и др. ...Клин. медицина.- 1986.- Т. 10.- С. 131–133.
Поршин К.К. и др. ...Архив патологии.- 1987.- Т. 29.- № 2.- С. 63–65.
Рыбаков С.И. Клиника диагностика и лечение гормонально-активных опухолей коркового вещества надпочечных желез: Дис. ... докт. мед. наук.- Киев, 1990.- 512 с.
Хирургия надпочечников. Под ред. А.П. Калинина, Н.А. Майстренко.- М.: Медицина, 2000.- 215 с.
Хитрова А.Н. Ультразвуковая диагностика заболеваний надпочечников/Клиническое руководство по ультразвуковой диагностике под ред. В.В. Митькова.- Т. I.- М.: Ю-Видап, 1996.- С. 302–311.
Эндокринология/Под ред. Н.Лавина. — М.: Практика, 1999.- 996 с.
Bvans H.L. et al. ...Am. J. Pathol.- 1996.- V. 105.- P. 76–86.
Fernandes-Cruz L. ...Brit. J. Surg.- 1966.- V. 83 (6).- P. 721–723.
Giron J. et al. ...Radiologie.- 1997.- V. 7 (4).- P. 225–232.
Gonczi I. et al. ...Radiol. diagn.- 1987.- V. 28 (5).- P. 643–650.
Gunhter R.W. et al. ...Clin. Ultrasound.- 1984.- V. 12.- P. 211–217.
Henry J.F. et al. ...J. Chir. (Paris).- 1996.- V. 133 (3).
Katz R.L. Kidney, adrenal and retroperitoneum/ Bibbo U. (ed.) Comprehensive cytopathology. — Philadelphia: W.B. Saunders, 1991.- P. 771–805.
Kohler R. et al. ...Acta Radiol. (Diagn), Stochholm, 4; 21–31 Jan, 1976.
Lack T.T. et al. (ed.) Pathology of the adrenal glands.- New York: Chyrchill Livingstont, 1990.- V. 14.- P. 115–163.
Medeiros L.J. et al. ...A review Am. J. Clin. Pathol.- 1992.- V. 97.- P. 73–83.
Mena A. et al. ...Endoscop. pract.- 1997.- V. 3 (2).- P. 98–105.
Nakao Y. et al. ...Nippon Jinzo Gakkai Shi.- 1993.- V. 35 (3).- P. 281–286.
Neville A.M. et al. Aspects of structure, function and pathology/ James V.H.T. (ed.) The agrenal gland.- New Jork: Raven Press, 1979.- P. 1–65.
Oelkers W. ...Europ. J. Endocr.- 1995.- V. 132.- P. 419–421.
Petronio R. et al. Fine needle aspiration biopsy of adrenal masses//31-st Congress of International society of surgery, Paris, Sept. 1–5, 1985.- 416 p.
Simon I. et al. ...Med. Clin.- 1991.- V. 15 (97).- P. 569–572.
Travis W.D. et al. Yiscellaneous tumors and tumefactive lesions of the adrenal glands/ Lack E.E. (ed.) Pathology of the adrenal gland.- New York: Cyurclill Livingstont, 1990.- V. 14.- P. 362–364.
Van Slooten H. et al. ...Cancer.- 1985.- V. 55.- P. 766–773.
Zografos G.C. et al. ...J. Surg. Oncol.- 1994.- V. 55 (3).- P. 160–164.
Описание проверено экспертом
Оцените статью:
- Опухоли надпочечника
- Кортикостерома
- Неоперабельные кортикостеромы
- Глюкостерома
Полужирным шрифтом выделены лекарства, входящие в справочники текущего года. Рядом с названием препарата может быть указан ежегодный уровень индекса информационного спроса (показатель, который отражает степень интереса потребителей к информации о лекарстве).
новообразование надпочечника
опухоль надпочечников, опухолями мозгового слоя надпочечников, наличии хромаффинных опухолей надпочечников,



