- Общие сведения
- Основные принципы диагностики опухолей костей
- Основные принципы лечения опухолей костей
- Доброкачественные опухоли костей
- Остеома
- Остеоид-остеома
- Остеобластома
- Хондрома
- Костно-хрящевой экзостоз (остеохондрома)
- Хондробластома
- Хондромиксоидная фиброма
- Гигантоклеточная опухоль
- Гемангиома
- Опухолеподобные поражения
- Солитарная (юношеская) костная киста
- Аневризмальная костная киста
- Эозинофильная гранулема
- Прочие опухоли
- Хордома
- Злокачественные опухоли костей
- Остеосаркома
- Паростальная (юкстакортикальная) остеосаркома
- Хондросаркома
- Саркома Юинга
- Фибросаркома кости
- Злокачественная фиброзная гистиоцитома (ЗФГ)
C40 Злокачественное новообразование костей и суставных хрящей конечностей, МКБ-10
- C40.0 Лопатки и длинных костей верхней конечности
- C40.1 Коротких костей верхней конечности
- C40.2 Длинных костей нижней конечности
- C40.3 Коротких костей нижней конечности
- C40.8 Поражение костей и суставных хрящей конечностей, выходящее за пределы одной и более вышеуказанных локализаций
- C40.9 Костей и суставных хрящей конечности неуточненной локалиации
Отредактировано: 02.04.2024
д.м.н., проф. Алиев М.Д., д.м.н. Харатишвили Т.К., к.м.н. Мачак Г.Н., к.м.н. Хатырев С.А.
ГУ РОНЦ им. Н.Н. Блохина РАМН
Общие сведения
Первичные опухоли костей встречаются сравнительно редко. Их частота не превышает 1% от всех злокачественных новообразований человека. По литературным данным, заболеваемость первичными опухолями костей в среднем составляют у мужчин 1, а у женщин 0,6–0,7 на 100 000 населения. Принято считать, что доброкачественные опухоли костей встречаются в 1–2,5 раза реже злокачественных опухолей костей. Опухоли костей в большинстве случаев возникают у людей молодого и среднего возраста. Чаще всего поражаются длинные трубчатые кости и кости таза. Этиология и патогенез первичных опухолей костей окончательно не выяснены.
Вторичные опухоли костей являются, как правило, результатом малигнизации таких заболеваний как костно-хрящевой экзостоз, множественный хондроматоз костей, деформирующий остеоз и др. Лиц, страдающих этими заболеваниями, следует относить к группе риска. В связи с редкостью возникновения, отсутствием в больничной сети специализированных отделений, а также в связи с тем, что опухоли костей не учитываются в статистических отчетах как самостоятельная нозологическая форма, многие проблемы их ранней диагностики и лечения остаются малоизученными. Наибольший опыт в области онкоостеологии в нашей стране накоплен в ГУ РОНЦ им. Н.Н. Блохина РАМН.
В настоящее время наиболее точно отвечает требованиям клиники гистологическая классификация ВОЗ первичных опухолей и опухолеподобных заболеваний костей:
I. Костеобразующие опухоли.
A. Доброкачественные опухоли.
1. Остеома.
2. Остеоид-остеома и остеобластома.
Б. Промежуточные.
1. Агрессивная (злокачественная) остеобластома.
В. Злокачественные.
Остеосаркома:
а) центральная (медуллярная);
б) поверхностная (периферическая):
паростальная,
периостальная,
поверхностная остеосаркома высокой степени злокачественности.
II. Хрящеобразующие опухоли:
A. Доброкачественные.
1. Хондрома:
а) энхондрома;
б) периостальная (юкстакортикальная).
2. Остеохондрома (костно-хрящевой экзостоз):
а) солитарный;
б) множественный.
3. Хондробластома (эпифизарная хондробластома).
4. Хондромиксоидная фиброма.
Б. Злокачественные.
1. Хондросаркома (первичная, вторичная).
2. Дедифференцированная хондросаркома.
3. Юкстакортикальная (периостальная) хондросаркома.
4. Мезенхимальная хондросаркома.
5. Светлоклеточная хондросаркома.
6. Злокачественная хондробластома.
III. Гигантоклеточная опухоль (остеокластома).
IV. Костномозговые опухоли (круглоклеточные опухоли).
1. Саркома Юинга костей.
2. Примитивная нейроэктодермальная опухоль кости (PNET).
3. Злокачественная лимфома кости (лимфосаркома).
4. Миелома.
V. Сосудистые опухоли.
A. Доброкачественные.
1. Гемангиома.
2. Лимфангиома.
3. Гломусная опухоль.
Б. Промежуточные или неопределенные.
1. Гемангиоэндотелиома (эпителиоидная гемангиоэндотелиома, гистиоцитоидная гемангиома).
2. Гемангиоперицитома.
В. Злокачественные.
1. Ангиосаркома (злокачественная гемангиоэндотелиома, гемангиосаркома, гемангиоэндотелиосаркома).
VI. Другие соединительнотканные опухоли.
A. Доброкачественные.
1. Доброкачественная фиброзная гистиоцитома.
2. Липома.
Б. Промежуточные.
1. Десмопластическая фиброма.
Б. Злокачественные.
1. Фибросаркома.
2. Злокачественная фиброзная гистиоцитома
3. Липосаркома.
4. Злокачественная мезенхимома.
5. Лейомиосаркома.
6. Недифференцированная саркома.
VII. Прочие опухоли.
A. Доброкачественные.
1. Нейролеммома.
2. Нейрофиброма.
Б. Злокачественные.
1. Хордома.
2. Адамантинома.
VIII. Опухолеподобные поражения.
1. Солитарная костная киста (простая или однокамерная).
2. Фиброзная дисплазия
3. Аневризмальная костная киста.
4. Юкстаартикулярная костная киста (внутрикостный ганглион).
5. Метафизарный фиброзный дефект (неоссифицирующая фиброма).
6. Эозинофильная гранулема (солитарная).
7. “Оссифицирующий миозит”.
8. “Бурая опухоль” гиперпаратиреоидизма.
9. Внутрикостная эпидермальная киста.
10. Гигантоклеточная (репаративная) гранулема.
Для стадирования заболевания и определения тактики лечения используется классификация по системе TNM.
Критерий T — первичная опухоль:
ТХ — недостаточно данных для оценки первичной опухоли;
Т0 — первичная опухоль не определяется;
Т1 — опухоль ограничена кортикальным слоем;
Т2 — опухоль распространяется за кортикальный слой.
Критерий N — регионарные лимфатические узлы:
NХ — недостаточно данных для определения регионарных лимфатических узлов;
N0 — нет признаков метастатического поражения регионарных лимфатических узлов;
N1 — регионарные лимфатические узлы поражены метастазами.
Критерий M — отдаленные метастазы:
МХ — недостаточно данных для определения отдаленных метастазов;
М0 — нет признаков отдаленных метастазов;
М1 — имеются отдаленные метастазы.
Также учитывается степень дифференцировки опухоли (критерий G):
GХ — степень дифференцировки не может быть установлена;
G1 — высокая степень дифференцировки;
G2 — средняя степень дифференцировки;
G3 — низкая степень дифференцировки;
G4 — недифференцированные опухоли.
Таблица 1
Группировка опухолей костей по стадиям
| Стадия IA | G1,2 | T1 | N0 | M0 |
| Стадия IB | G1,2 | T2 | N0 | M0 |
| Стадия IIA | G3,4 | T1 | N0 | M0 |
| Стадия IIB | G3,4 | T2 | N0 | M0 |
| Стадия III | Не определяется | |||
| Стадия IVA | Любая G | Любая T | Любая N | Любая M |
| Стадия IIIB | Любая G | Любая T | Любая N | Любая M |
Широкое распространение в научно-практической литературе получила и классификация, разработанная американским исследователем W. Enneking (табл. 2)
Таблица 2
Стадирование опухолей костей по Enneking
| Стадия IА | G1,2 | T1 | M0 |
| Стадия IB | G1,2 | T2 | M0 |
| Стадия IIА | G3,4 | T1 | M0 |
| Стадия IIB | G3,4 | T2 | M0 |
| Стадия IIIA | G3,4 | T1 | M1 |
| Стадия IIIB | G3,4 | T2 | M1 |
Основные принципы диагностики опухолей костей
Основными клиническими признаками опухолей костей являются боли и (или) наличие неподвижного относительно кости опухолевого образования, а также нарушение функции пораженной конечности. Для первичных злокачественных новообразований костей характерны упорные, прогрессирующие, усиливающиеся по ночам боли, которые плохо и на короткое время купируются анальгетиками. Применяемая до установления диагноза физиотерапия нередко усиливает боли и темпы роста опухоли, хотя иногда снижает на короткий промежуток времени интенсивность болей.
При подозрении на опухоль кости больной подлежит полному клинико-инструментальному обследованию. Важнейшим и наиболее доступным методом ранней диагностики является рентгенологическое исследование, которое начинается с рентгенографии пораженной кости в двух стандартных проекциях. При болях в области коленного сустава и отсутствии изменений на рентгенограммах необходимо произвести снимки костей таза с тазобедренными суставами, т.к. часто при поражении области тазобедренного сустава боли иррадиируют в коленный сустав. Рентгенограммы должны быть хорошего качества и расшифровываться рентгенологом, имеющим подготовку по костной патологии. Обращают внимание на локализацию очага поражения, состояние кортикального слоя, наличие зоны склероза вокруг опухоли, характер и выраженность периостальной реакции. В специализированных учреждениях, для уточняющей диагностики, определения стадии заболевания и выработки тактики лечения проводится ряд дополнительных исследований (АГ, КТ и МРТ, радиоизотопное сканирование скелета). При возникновении сомнений в диагнозе и невозможности полностью исключить костную опухоль показано повторное рентгенологическое обследование через 2–4 нед.
Лабораторные методы исследования помогают в проведении дифференциального диагноза с воспалительными, инфекционными (туберкулез) процессами, остеодистрофиями (паратиреоидная) и некоторыми другими заболеваниями.
Клинико-рентгенологический диагноз обязательно должен быть подтвержден данными морфологического исследования. Производится трепан— или открытая биопсия опухоли.
Для правильной интерпретации патологического процесса в кости необходима совместная работа клинициста, рентгенолога и патолога, специализирующихся в области костной патологии.
Основные принципы лечения опухолей костей
Тактика лечения больных с первичными опухолями костей зависит от нескольких факторов:
1. Во-первых, это гистологическая форма опухоли.
В лечении доброкачественных опухолей ведущим методом является хирургический. Злокачественные опухоли костей представляют собой разнородную группу нозологических форм, отличающихся по биологическим характеристикам, клиническими проявлениями, способностью к метастазированию, рецидивированию, чувствительностью к химиотерапии и лучевым методам воздействия. Так, например, хондросаркомы низкой степени злокачественности не чувствительны к химиолучевой терапии, и для них единственным методом лечения является радикальное хирургическое вмешательство. В то же время, такие опухоли как остеосаркома, злокачественная фиброзная гистиоцитома, саркома Юинга, низкодифференцированные хондросаркомы отличаются склонностью к ранней гематогенной диссеминации. Поэтому, лечение этих нозологических форм должно быть комплексным и предусматривать, помимо локального воздействия, т.е. операции или лучевой терапии, также и воздействие на субклинические метастазы: с этой целью проводится химиотерапия.
2. Вторым определяющим фактором при выборе тактики лечения является стадия заболевания.
При наличии явных отдаленных метастазов, на первый план выходят лекарственные методы. В дальнейшем, в зависимости от характера ответа на проводимую терапию, в лечебную программу вносятся необходимые коррективы. При выраженном ответе возможно хирургическое лечение первичной опухоли, а также удаление ее отдаленных метастазов.
3. Третьим важнейшим моментом при выборе тактики лечения является определение объема хирургического вмешательства.
Главным условием операции при саркомах костей является радикальность удаления опухоли, которая должна в дальнейшем гарантировать отсутствие местного рецидива. Радикальным считается удаление опухоли в пределах слоя здоровых мышечных тканей, отсутствие опухолевых клеток по линии костного спила, исключение вскрытия опухолевой псевдокапсулы.
Вид операции определяется в зависимости от возраста больного, гистологической формы опухоли, степени ее местной распространенности, вовлечения близлежащих сосудисто-нервных образований, характера ответа на предоперационное лечение. Хирургические вмешательства при саркомах костей могут быть калечащими (ампутации, экзартикуляции) и сохраняющими конечность. Калечащие операции показаны при местно-распространенных саркомах, вовлекающих магистральные сосуды и нервы, кожу, при существовании угрозы распада опухоли. В остальных случаях в первую очередь следует рассматривать возможность выполнения сохранной операции. И тот, и другой тип оперативных вмешательств должны быть выполнены радикально и абластично. Это означает, что злокачественная опухоль удаляется с мышечно-фасциальным влагалищем, операция производится на вышележащем сегменте конечности с пересечением ее выше места прикрепления мышц, переходящих с пораженного на непораженный сегмент конечности (принцип футлярности). При радикальной резекции опухоль также удаляется с мышечно-фасциальным влагалищем. В зоне, где граница футляра технически недоступна, опухоль удаляется со значительным слоем окружающих ее мышц (принцип зональности).
Применяемая в последние годы предоперационная химиотерапия, может уменьшить размеры опухоли, способствовать ее отграничению псевдокапсулой, перевести ее из ампутабельной формы в резектабельную. Образовавшиеся после сегментарных резекций костные дефекты замещают с помощью металлических эндопротезов или костными трансплантатами. Существенно улучшаются исходы костной пластики при пересадке васкуляризированных трансплантатов с применением микрохирургической техники и внеочаговой фиксации аппаратом Илизарова.
Лучевая терапия имеет ограниченное самостоятельное значение и используется только в сочетании с химиотерапией или в качестве предоперационной подготовки при ряде радиочувствительных сарком костей. Метод облучения, доза и источник облучения зависят от возраста больного, локализации и размеров опухоли и характера планируемого оперативного вмешательства.
Основные этапы эволюции методов лечения злокачественных опухолей костей приведены в таблице 3.
Таблица 3
Эволюция методов лечения злокачественных опухолей костей
| 50-е гг. XX в. |
60–70-е гг. XX в. |
80–90-е гг. XX в. |
С 2000 г. |
| Ампутационная хирургия | Ампутационная хирургия | Неоадъювантная химиотерапия | Современная неоадъювантная химиотерапия |
| Лучевая терапия | Адъювантная химиотерапия | Органосохраняющие операции у 50-60% больных | Органосохраняющие операции — 85-90%, комбинированное лечение метастатических опухолей костей |
| Выживаемость до 10% | Выживаемость до 40% | Выживаемость до 55% | Выживаемость до 75% |
Доброкачественные опухоли костей
Остеома
Выделяют компактную и губчатую формы. Микроскопически компактная остеома состоит почти сплошь из костной массы тонковолокнистой или пластинчатой с очень узкими сосудистыми каналами. Губчатая остеома, напротив, представлена четкой сетью костных балок, но расположенных беспорядочно.
Опухоль характеризуется длительным бессимптомным течением и очень медленным ростом. Как правило, является случайной рентгенологической находкой. Компактная остеома преимущественно локализуется в костях черепа (гайморова пазуха, лобная пазуха, решетчатый лабиринт), реже — в позвонках. Губчатая и смешанные формы остеомы, как правило, локализуются в метафизарных или метадиафизарных отделах. В процессе роста отодвигается от зоны роста. При значительных размерах может пальпироваться как безболезненное неподвижное образование костной плотности.
Рентгенологически компактная остеома характеризуется дополнительным образованием небольших размеров, большой плотности с четкими контурами в проекции придаточных пазух или задних отделов позвонков. Возможны множественные остеомы.
Губчатая или смешанные остеомы напоминают по рентгенологической картине остеохондрому или костно-хрящевой экзостоз, исходящий из метафизарных или метадиафизарных отделов с широкой ножкой, имеющий четкий контур, без наличия обызвествлений. В отличие от остеохондромы не имеет хрящевого покрытия.
Ввиду клинико-рентгенологической схожести с остеохондромой, окончательный диагноз ставится с учетом гистологического исследования.
Лечение. При росте опухоли показана краевая резекция кости.
Остеоид-остеома
Микроскопически опухоль представляет собой картину весьма активной перестройки костной ткани. Можно выделить несколько своеобразных клеточно-тканевых зон. Центральные отделы содержат большое количество клеток в виде скопления молодых сочных остеобластов и тонкостенных кровеносных сосудов. Вблизи центра опухоли обычно видны массы остеоида. Периферические участки состоят из зрелых костных балок. Затем следует зона остеосклероза.
Клиника характеризуется длительными, упорными ночными болями, проходящими при приеме анальгетиков, с постепенно повышающейся до нескольких таблеток в день дозировкой. Несмотря на длительное течение, интенсивность болей не нарастает. Процесс, как правило, локализуется в диафизах и метадиафизах длинных трубчатых костей. Возможна локализация в коротких трубчатых, губчатых костях плоских костях. У мужчин во втором-третьем десятилетиях жизни встречается в 4–5 раз чаще.
На рентгенограммах характерен остеолитический очаг небольших размеров, округлой или овальной формы, отграниченный от неизмененной костной ткани широкой зоной склероза с наличием очага просветления в центре (гнездо остеоид-остеомы). Очаг деструкции часто сопровождается утолщением кортикального слоя за счет частично слившихся периостальных наслоений. В ряде случаев для выявления гнезда остеоид-остеомы показаны: рентгенография “жесткими лучами”, КТ или МРТ. При локализации остеоид-остеомы в губчатых костях характерен остеосклероз вокруг гнезда и отсутствие периостальной реакции. Дифференциальный диагноз следует проводить с воспалительными процессами — кортиколитами.
Лечение хирургическое: краевая резекция с обязательным удалением гнезда остеоид-остеомы. Показателем удаления гнезда является исчезновение характерных для остеоид-остеомы болей в первый послеоперационный день.
Остеобластома
Микроскопически остеобластома не имеет принципиальных различий с остеоид-остеомой и обычно представлена элементами незрелой тонко— и грубоволокнистой кости, массами остеоида, тонкостенными сосудами и весьма варьирующим количеством клеток типа остеобластов, остеокластов и фибробластов.
Клиника. Характерны длительные интенсивные боли, преимущественно в ночное время. При локализации в позвоночнике возможна иррадиация болей в суставы нижних конечностей (тазобедренный, коленный). Боли снимаются или значительно облегчаются приемом анальгетиков. Течение заболевания длительное (годами до рентгенологического выявления очага деструкции кости).
Излюбленная локализация в дужках позвонков, костях запястья, предплюсны, редко — в длинных трубчатых костях. Наиболее часто встречается во втором-третьем десятилетиях жизни.
При локализации опухоли в костях кисти и стопы отмечается увеличение объема мягких тканей над очагом деструкции, болезненное при пальпации. При локализации опухоли вблизи сустава возможно нарушение его функции (ограничение движений). При локализации опухоли в позвоночнике отмечается ограничение подвижности, выпрямление физиологических искривлений, возможны боли радикулярного характера.
На рентгенограммах характерен литический очаг деструкции округлой формы с четкими, возможно фестончатыми, контурами, отграниченный от смежных отделов костной ткани узкой зоной склероза. Опухоль вызывает истончение и вздутие кортикального слоя. Мягкие ткани над очагом увеличены в объеме. Возможны участки обызвествления в проекции очага деструкции. При локализации в позвоночнике опухоль чаще поражает элементы дужки (корень дужки, поперечный отросток, суставные отростки). При этом на рентгенограммах, как правило, выявляется очаг деструкции литического характера, вызывающий вздутие кортикального слоя вышеуказанных элементов позвонка. Значительную помощь в визуализации опухоли оказывают КТ и МРТ. При значительных размерах опухоли возможен разрыв кортикального слоя с выходом опухоли в окружающие мягкие ткани. При сходной клинической картине с остеоид-остеомой в рентгенологическом отображении остеобластома отличается большими размерами, отсутствием гнезда и менее выраженными периостальными наслоениями. Описаны случаи озлокачествления с формированием вторичной остеосаркомы.
Лечение хирургическое — краевая или сегментарная резекция кости с ауто— или аллопластическим замещением дефекта.
Хондрома
Редко встречающаяся солитарная доброкачественная хрящевая опухоль, источником роста которой является необызвествившийся в процессе оссификации скелета участок хрящевой ткани или участок эктопированной эмбриональной хрящевой ткани в костях, не проходящих хрящевую стадию формирования (ключица и др.). Множественные хондромы развиваются вторично у больных, страдающих врожденным диспластическим процессом — множественным хондроматозом костей (болезнь Олье). Хондромы чаще всего локализуются в костях кисти и стопы, реже в метафизарных отделах длинных трубчатых костей, плоских костях.
Клиника. Течение большинства хондром бессимптомное. Могут беспокоить периодически возникающие ноющие боли в близлежащем суставе, возможно длительное бессимптомное течение, при котором первым проявлением заболевания может быть, патологический перелом. Признаком опухолевого превращения очага болезни Олье является начавшийся его рост, при этом может происходить опухолевая трансформация одновременно в нескольких очагах дисхондроплазии. Хондромы могут озлокачествляться с образованием вторичных хондросарком, что чаще происходит в плоских костях, проксимальном отделе бедренной кости и чрезвычайно редко — в костях кисти и стопы.
На рентгенограммах отмечается остеолитический очаг деструкции, отграниченный от неизмененных отделов кости зоной склероза. Характерны участки обызвествления. Остеолитический очаг может иметь центральное расположение (энхондрома) или эксцентрическое расположение (экхондрома). В динамике при длительном наблюдении возможно истончение кортикального слоя и его вздутие без нарушения целостности. Патологический перелом при хондроме, как правило, срастается.
Патологическая анатомия. Макроскопически хондромы представляют собой обычно хорошо отграниченные опухоли округлой формы. Микроскопически ткань хондромы приближается к типу зрелого гиалинового хряща. От нормального гиалинового хряща хондромы отличаются беспорядочным расположением клеток. Хондромы из волокнистого хряща исключительно редки.
Лечение. Только хирургическое — краевая или реже сегментарная резекция кости с ауто— или аллопластикой дефекта. Операция должна быть радикальной и абластичной, т.к. нередко такая опухоль уже является вторичной хондросаркомой. Прогноз благоприятный, но при нерадикальном удалении есть склонность к рецидивам и озлокачествлению, кроме энхондром кисти, которые практически не рецидивируют.
Костно-хрящевой экзостоз (остеохондрома)
Достаточно частое заболевание костной системы, которое вероятнее всего представляет собой порок развития и может быть связано с наследственными факторами. Возникает практически в любой кости, которая проходит хрящевую фазу развития. Остеохондрома состоит из костного основания и его хрящевого покрытия. Интенсивный рост экзостоза или возобновление его роста после остановки роста скелета характеризует его превращение в хрящевую опухоль — хондрому или вторичную хондросаркому, т.е. опухолевая трансформация экзостоза происходит только за счет его хрящевого покрытия.
Патологическая анатомия. Остеохондромы представляют собой костные выросты с хрящевым покрытием. Хрящевая ткань имеет строение гиалинового хряща, но обычно клетки в нем располагаются беспорядочно. Нередко у молодых лиц строение хряща приближается к строению хондромы. Обычно хрящевое покрытие не отграничено от костной ткани субхондральной костной пластинкой, и хрящевая ткань продолжается в подлежащую костную ткань экзостоза в виде нерегулярно расположенных участков.
Клиника. Характерно наличие единичных или множественных образований костной плотности разной величины (от нескольких до десятков сантиметров), локализующихся в метафизе длинной трубчатой кости или в плоских костях и неподвижных по отношению к кости. Как правило, опухоль безболезненна. При ее больших размерах могут ограничиваться движения в близлежащем суставе. Рост опухоли медленный и прекращается с ростом организма. Клинические размеры приблизительно соответствуют рентгенологическим. Чаще всего локализуется в метафизарных отделах плечевой, большеберцовой и бедренной костей, но может встречаться в подвздошной кости, лопатке и позвоночнике. Большинство больных в возрасте до 20 лет. Несколько чаще болезнь проявляется у лиц мужского пола. При множественных экзостозах целесообразна консультация генетика.
На рентгенограммах определяется изменение формы кости за счет наличия дополнительного образования, исходящего тонкой или широкой ножкой. Контур кортикального слоя четкий, плавно переходит в основание ножки. Дистальные отделы образования имеют неровный контур. Возможны известковые вкрапления. Иногда отмечается увеличение объема мягких тканей над образованием и оттеснение мышечных групп. Клинико-рентгенологическая картина настолько характерна, что, как правило, нет необходимости в дифференциальном диагнозе.
Озлокачествление солитарных остеохондром отмечается в 1–2% случаев, множественных остеохондром — в 5–10% случаев, чаще — при локализации в костях таза и лопатке. Малигнизация данной опухоли проявляется заметным ускорением ее роста, иногда появлением болей. На рентгенограммах появляются размытость контуров, увеличение обызвествлений в мягкотканном компоненте опухоли. Характерно значительное несоответствие клинических и рентгенологических размеров опухоли (клинические размеры значительно больше), что объясняется наличием рентгенопрозрачного хрящевого компонента, за счет которого и растет опухоль. В случае озлокачествления, используется тактика лечения хондросаркомы.
Лечение. Единственным методом лечения является хирургический — краевая резекция кости с обязательным удалением основания ножки экзостоза. Пластики краевого дефекта кости не требуется. Оперативное лечение показано в случае начала роста опухоли или когда остеохондрома ограничивает движения в близлежащем суставе. В остальных случаях показано динамическое наблюдение.
Прогноз заболевания хороший. После удаления остеохондромы наступает выздоровление.
Хондробластома
Является сравнительно редкой опухолью, возникающей во втором, реже — в третьем десятилетии жизни, чаще у мужчин. Характерна локализация в эпифизах и эпиметафизах длинных трубчатых костей.
Патологическая анатомия. Микроскопически опухоль построена из клеток полицилиндрической или округлой формы. Границы клеток неотчетливы, ядро крупное. Могут быть митозы, обычно немногочисленные. Характерной принадлежностью хондробластом является наличие многоядерных клеток остеокластического типа. Они часто разбросаны в опухоли одиночно или группами, а иногда образуют вместе с одноядерными клетками опухоли ткань типа гигантоклеточной опухоли.
Клиника. Характерна длительно существующая, непостоянной интенсивности боль ноющего характера. Часто отмечается нарушение функции близлежащего сустава, а также наличие выпота в суставе, повышение местной температуры над опухолью. Течение заболевания длительное. При адекватном хирургическом вмешательстве не рецидивирует.
На рентгенограммах выявляется эксцентрически расположенный бесструктурный очаг деструкции литического характера округлой или овальной формы с участками крапчатого обызвествления (приблизительно в половине случаев), локализующийся, в подавляющем большинстве случаев, в эпифизарном отделе. При незакрытой зоне роста возможно ее разрушение опухолью и распространение процесса на область метафиза. Очаг деструкции отграничен от неизмененных отделов кости зоной склероза. В процессе роста опухоли происходит истончение, вздутие кортикального слоя. Возможно истончение и вздутие замыкательной пластинки эпифиза, иногда появляются слившиеся периостальные наслоения в области метафиза кости. Суставная щель может быть расширена в связи с выпотом в суставе. В динамике отмечается увеличение очага деструкции, истончение и, вздутие кортикального слоя (замыкательная пластинка эпифиза).
Хондробластому необходимо отдифференцировать от хондросаркомы и гигантоклеточной опухоли. Отличительными особенностями хондробластомы являются молодой возраст больного, эпифизарная локализация опухоли, наличие зоны склероза вокруг опухоли, отсутствие периостальной реакции, наличие мелких очагов обызвествления.
Лечение хирургическое и заключается в околосуставной резекции с ауто— или аллопластическим замещением дефекта кости. При опухолях больших размеров с разрушением кортикального слоя кости или при рецидивных опухолях показана резекция суставного конца длинной трубчатой кости с ауто— или аллопластикой дефекта, возможно также эндопротезирование.
При рецидивной хондробластоме необходима консультация гистологических препаратов в специализированном учреждении для исключения светлоклеточной хондросаркомы. Прогноз благоприятный.
Хондромиксоидная фиброма
Патологическая анатомия. Макроскопически ткань опухоли имеет сероватый оттенок, консистенция ее плотноватая. Микроскопически опухоль обычно представляется разделенной на дольки тяжами более мелких клеток, группирующихся вокруг сосудов капиллярного и синусоидного характера. Клетки опухоли многочисленны, в основном мелкие, имеют вытянутую или звездчатую форму и заключены в однородное межклеточное вещество.
Клиника. Возможно длительное бессимптомное течение. Первым симптомом является деформация кости, появление припухлости. Чаще встречается в детском и подростковом возрасте (второе десятилетие жизни). Локализуется в метафизах длинных трубчатых костей, возможна локализация в костях таза (чаще всего в крыле подвздошной кости, вблизи крестцово-подвздошного сочленения). Боли умеренно выраженные, ноющего характера.
На рентгенограммах определяется эксцентрически расположенный очаг деструкции, отграниченный от смежных отделов неизмененной кости зоной склероза. Контуры очага четкие и ровные, возможна фестончатость контуров. Очаг может истончать и “вздувать” кортикальный слой. При незакрытой зоне роста возможно ее разрушение опухолью. Вкрапления известковой плотности в проекции очага деструкции встречаются очень редко и не характерны для этой опухоли. Случаи озлокачествления чрезвычайно редки и описываются как казуистика. Озлокачествления хондромиксоидной фибромы у детей не описаны.
Лечение хирургическое в объеме краевой резекции кости. При больших размерах образующегося дефекта кости показано его ауто— или аллопластическое замещение.
Гигантоклеточная опухоль
В группу гигантоклеточных опухолей до недавнего времени включались юношеские костные кисты. Истинные гигантоклеточные опухоли у детей до 16 лет возникают весьма редко и протекают как опухоли высокого злокачественного потенциала с плохим прогнозом. С другой стороны, патоморфологические работы последних лет установили значительное морфологическое сходство отдельных форм опухоли со злокачественной фиброзной гистиоцитомой. Частота метастазирования гигантоклеточной опухоли не превышает 5%.
Патологическая анатомия. Микроскопически опухоль состоит в основном из клеток двух типов. Преобладают слегка вытянутые клеточные элементы с округлым или овальным ядром, среди которых более или менее равномерно распределены многоядерные гигантские клетки, содержащие иногда до 50–100 ядер. Иногда встречаются типичные фигуры митоза. Кроме этого, в составе гигантоклеточной опухоли регулярно встречаются участки с фибробластами и большей или меньшей продукцией коллагена, поля ксантомных клеток и участками кровоизлияний.
Клиника. Характерны умеренной интенсивности боли, усиливающиеся при физической нагрузке, возможны ночные боли, нарушение функции близлежащего сустава. Возраст больных — третье-четвертое десятилетия жизни. Длительность течения от нескольких месяцев до 2 лет. Локализуется опухоль в метаэпифизах длинных трубчатых костей (около 50% — в костях, формирующих коленный сустав), реже встречается в костях таза, крестце, позвоночнике, губчатых костях. При больших размерах опухоли бывает нарушение конфигурации сустава, возможно усиление сосудистого рисунка, ограничение движений в суставе, пальпируется дополнительное болезненное образование костной плотности. Нередко встречается уменьшение объема конечности (атрофии мышц). Возможны патологические переломы, которые могут срастаться при иммобилизации. Гигантоклеточная опухоль способна к рецидивам, в т.ч. и в окружающие кость мягкие ткани, к метастазированию в отдаленные органы, к озлокачествлению доброкачественных форм.
Выделяются доброкачественные гигантоклеточные опухоли со спокойным течением (рентгенологически — ячеистая фаза) и более агрессивным (рентгенологически — литическая фаза). Злокачественные формы: первично злокачественная, озлокачествленная (вторично злокачественная) и метастазирующая с доброкачественной анатомической структурой.
Рентгенологически гигантоклеточная опухоль характеризуется наличием очага деструкции, в большинстве случаев центрально расположенного в метаэпифизарных отделах длинных трубчатых костей, отграниченного от неизмененной ткани слабо выраженной зоной склероза, которая зависит от длительности существования и скорости роста опухоли (чем выраженнее склероз, тем медленнее растет и длительнее существует опухоль, что свидетельствует о доброкачественности процесса) (рис. 1). Очаг деструкции при значительных размерах опухоли вызывает истончение и вздутие кортикального слоя. Возможно разрушение кортикального слоя с выходом опухоли в экстраоссальные мягкие ткани, что указывает на возможность инфильтрирующего роста. Очаг деструкции нередко имеет ячеистое строение. Остеолитическая деструкция свидетельствует о более агрессивном течении опухоли. Гигантоклеточная опухоль относится к условно доброкачественным опухолям. Возможно озлокачествление опухоли. Частота озлокачествление возрастает после лучевой терапии в дозе более 40 Гр и при рецидивах после нерадикальных операций. Рентгенологические признаки озлокачествления гигантоклеточной опухоли: быстрое увеличение преимущественно остеолитического очага деструкции с потерей четкости контуров и исчезновением зоны склероза, с разрушением кортикального слоя, возможным его разволокнением и появлением козырька Кодмена и экстраоссального компонента опухоли. КТ и МРТ вносят дополнительную информацию о степени распространенности опухоли, необходимую при планировании хирургического лечения. Возможны единичные и множественные метастазы в легкие.
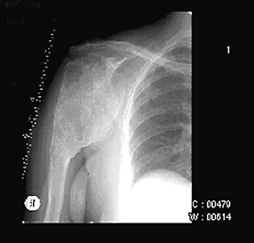
Рисунок 1. Рентгенологическая картина гигантоклеточной опухоли проксимального отдела плечевой кости
Лечение хирургическое. При доброкачественных формах с ячеистой структурой и ограниченными размерами патологического очага, спокойным клиническим течением производится околосуставная краевая резекция с электрокоагуляцией стенок костной полости и алло— или аутопластикой дефекта. Эти больные требуют в дальнейшем тщательного динамического наблюдения для своевременного выявления возможного рецидива опухоли.
При литических формах с выраженной клинической картиной и при больших размерах патологического очага производится сегментарная резекция суставного конца кости с эндопротезированием или аллопластикой дефекта кости.
Процент рецидивов и метастазов возрастает в несколько раз при разрушении кортикального слоя кости, выходе опухоли в мягкие ткани и наличии патологического перелома. В таких ситуациях может быть показана предоперационная лучевая терапия. Лучевая терапия может использоваться при локализации опухоли в позвоночнике, крестце и при некоторых других локализациях, при которых радикальное и абластичное удаление опухоли затруднено. Доза не должна превышать 40 Гр. Эти больные нуждаются в тщательном и длительном динамическом наблюдении.
5-летняя выживаемость при гигантоклеточной опухоли составляет 96%. Частота рецидивирования зависит от объема оперативного вмешательства: при сегментарной резекции — 19%, при краевой резекции — 29%, при экскохлеации — 46%.
Гемангиома
Доброкачественная сосудистая опухоль, характеризующаяся длительным бессимптомным течением. Встречается в любом возрасте. Преимущественно поражает тела позвонков и кости свода черепа. При значительных размерах опухоли возможно появление болей при физической нагрузке.
Рентгенологически гемангиома характеризуется диффузным лучистым или мелкоочаговым изменением структуры кости. Кортикальньй слой не поражается, периостальных реакций нет. Участки измененной структуры отграничены зоной выраженного склероза. При локализации в теле позвонка гемангиома характеризуется вертикально расположенными утолщенными костными балками. При этом могут поражаться тела смежных позвонков. Возможно изменение структуры в виде мелкоочаговых участков разрежения, отграниченных выраженной зоной склероза. Возможно поражение задних отделов дужки. Часто встречаются патологические переломы, при которых изменяется характер структуры, что делает возможной постановку правильного диагноза только в динамике.
Лечение. Основным методом лечения является лучевая терапия. При отсутствии клинических симптомов и случайном выявлении гемангиомы кости лечение не проводится. Лучевая терапия показана при появлении неврологических симптомов, обусловленных давлением опухоли на спинной или головной мозг, поскольку основной локализацией костных гемангиом являются позвонки или кости черепа. Облучение дистанционное, проводят РОД 1,6–2 Гр, в СОД 20–35 Гр. В результате лечения наблюдается исчезновение клинических симптомов, которое может происходить быстро или на протяжении 4–6 мес.
Опухолеподобные поражения
Солитарная (юношеская) костная киста
Ранее ошибочно трактовалась как конечная фаза развития гигантоклеточной опухоли. В подавляющем большинстве случаев течение бессимптомное. Выявляется как случайная рентгенологическая находка или при патологическом переломе. Чаще наблюдается во втором десятилетии жизни. В процессе роста кисты возможно поражение зоны роста кости с появлением вторичной деформации сегмента конечности (относительно редко). Типичная локализация в метафизарных отделах длинных трубчатых костей (преимущественно плечевая и бедренная кости) с тенденцией распространения в сторону диафиза с отдалением зоны роста. Для течения кист характерна стадийность процесса (при динамическом наблюдении). Выделяют активную фазу, фазу отграничения и фазу репарации, или обратного развития.
Рентгенологически солитарная костная киста характеризуется участком разрежения кости с четкими контурами, иногда ячеистого строения, преимущественно центрально расположенного, округлой или овальной формы, отграниченного от неизмененной костной ткани зоной склероза. Кортикальный слой может быть истончен изнутри, возможно вздутие кортикального слоя без нарушения его непрерывности. Характерны патологические переломы, срастающиеся в обычные сроки с последующей репарацией кисты.
Активная фаза костной кисты характеризуется очагом разрежения, не везде четко отграниченным, округлой или овальной формы, расположенным вблизи зоны роста. Кортикальной слой истончен, циркулярно вздут. В динамике отмечается увеличение очага разрежения кости с возможным распространением как в сторону диафиза, так и в сторону зоны роста. Возможны повреждения зоны роста с последующим развитием деформаций кости. Характерны патологические переломы.
Фаза отграничения костной кисты: при динамическом контроле очаг разрежения не увеличивается или уменьшается в размерах, отграничивается широкой зоной склероза, кортикальный слой утолщается. После патологического перелома возможна частичная репарация кисты.
Фаза репарации: в процессе динамического наблюдения отмечается уменьшение размеров кисты с частичным восстановлением ее структуры. Появляются участки склероза, утолщение кортикального слоя за счет слившихся периостальных наслоений, смещение очага в сторону диафиза.
Аневризмальная костная киста
Клиническое течение медленное, спокойное, часто бессимптомное. Боли незначительные, в основном при ходьбе (при локализации в ноге), может встречаться нарушение функции близлежащего сустава. Встречается преимущественно в первом-втором десятилетиях жизни, реже — в третьем. Часто наблюдаются патологические переломы, которые консолидируются в обычные сроки. Может локализоваться во всех отделах скелета, но чаще в метадиафизах длинных трубчатых костей. Клиническое течение характеризуется стадийностью процесса. В течение заболевания выделены 3 фазы: активная, стабилизации, восстановления.
Важный дифференциально-диагностический признак: при пункции очага — истекающая под большим давлением кровь.
Активная фаза характеризуется наличием болей, припухлостью, повышением местной температуры, иногда пальпируется опухолевидное образование, чаще возникают патологические переломы. Рентгенологически выявляется солитарный очаг деструкции, расположенный эксцентрично, не связанный с зоной роста и нередко достигающий больших размеров, форма очага деструкции неправильная, контур нечеткий, зона склероза выражена умеренно, на отдельных участках может отсутствовать. Деструкция остеолитического характера, ячеистой структуры, над очагом возможен линейный периостит или слившиеся периостальные наслоения. Часто встречается вздутие кортикального слоя.
Фаза стабилизации (отграничения) характеризуется уменьшением клинической симптоматики и стабилизацией процесса. Рентгенологически очаг отграничивается выраженной зоной склероза на всем протяжении, утолщается кортикальный слой. Очаг в динамике уменьшается в размерах, усиливаются признаки репарации. В процессе роста больного очаг деструкции сдвигается в сторону диафиза.
Фаза восстановления. Клинически на первый план выходят деформации кости (укорочение, искривление). Рентгенологически костная структура восстанавливается, возможно наличие остаточных полостей небольших размеров после репарации аневризмальной костной кисты с последующим почти полным восстановлением костной структуры.
Лечение костных кист в подавляющем большинстве случаев консервативное.
В фазе остеолиза — 2–3 пункции кисты с интервалом 7–10 дней с введением склерозирующих лекарственных препаратов (после промывания аминокапроновой кислотой вводится 20000 ЕД апротинина). При длительно существующих кистах вводится гидрокортизон в дозе 40 мг (2 мл) или триамцинолон — 1 мл. В дальнейшем — динамическое наблюдение. При слабо выраженной положительной динамике — повторные лечебные пункции. Оперативное лечение в фазе остеолиза неэффективно и проводится только при распространении очага на зону роста, что вызывает ее преждевременное закрытие с последующим развитием укорочения и деформации конечности.
В фазе отграничения показано динамическое наблюдение. При больших размерах кисты — лечебные пункции. Оперативное лечение проводится по показаниям (большие размеры кисты, повторные переломы).
В фазе репарации также показано динамическое наблюдение. Оперативное лечение не показано. Возможны остаточные полости кисты, не требующие специального лечения.
Эозинофильная гранулема
Не являясь собственно опухолью, важна в плане проведения дифференциальной диагностики. Характеризуется наличием умеренных болей ноющего характера. Преимущественно встречается у детей и подростков, чаще — у мальчиков, редко — у взрослых. Возможно бессимптомное клиническое течение. В этом случае эозинофильная гранулема является случайной рентгенологической находкой. Не имеет излюбленной локализации, но чаще встречается в плоских (ребра, лопатка, подвздошная кость) и губчатых (тела позвонков) костях.
Рентгенологически эозинофильная гранулема характеризуется cтадийностью течения.
Активная фаза — остеолитический очаг деструкции без четких контуров с отсутствием зоны склероза. При близком расположении к кортикальному слою возможна периостальная реакция в виде линейного периостита.
Фаза отграничения характеризуется уменьшением размеров очага, появлением выраженной разлитой зоны склероза, периостальные наслоения склонны к ассимиляции и утолщению кортикального слоя.
Фаза восстановления — неравномерное восстановление костной структуры с участками склероза и утолщением кортикального слоя над очагом.
Изменения в позвоночнике также имеют стадийный характер от остеолитического очага в теле позвонка до равномерного снижения его высоты и появления равномерно уплощенного позвонка с уплотненной структурой — вертеброплана, причем выше и нижележащие межпозвонковые пространства остаются неизмененными.
Эозинофильная гранулема характеризуется клиническим и рентгенологическим полиморфизмом проявлений, что делает ее на разных этапах сходной с различными доброкачественными и злокачественными опухолями. При этом основой в постановке правильного диагноза является клиника и динамика рентгенологических изменений и морфологическая верификация процесса.
Лечение. Оперативная эксцизионная (тотальная) биопсия одновременно является и методом лечения. При локализации в хирургически труднодоступных зонах (позвоночник) может проводиться лучевая терапия (36–40 Гр).
Прочие опухоли
Хордома
Злокачественное новообразование, развивающееся из остатков примитивной эмбриональной спинной струны (хорды).
Клиника. Характеризуется длительным, довольно часто бессимптомным течением. Жалобы на периодические боли ноющего характера, малой интенсивности, не усиливающиеся к ночи. По мере роста опухоли клиническая картина определяется локализацией процесса в позвоночнике. Наиболее часто опухоль локализуется в области крестца (60–70%), где на первый план наряду с болями выходит нарушение функции тазовых органов. При осмотре через прямую кишку (через ее заднюю стенку) пальпируется плотно-эластической консистенции, умеренно болезненная при пальпации опухоль. Слизистая прямой кишки подвижна. На втором месте по частоте опухоль локализуется в шейных позвонках и основании черепа, где в клинической картине на первый план выходят общемозговые симптомы и симптомы сдавления (дислокации) мозга. При локализации в грудном и поясничном отделах позвоночника клиническая и неврологическая картина зависит от уровня поражения. У мужчин встречается более чем в 2 раза чаше, чем у женщин. Возраст — 40–50 лет.
При рентгенографии определяется очаг деструкции остеолитического характера, больших размеров с неровными, фестончатыми контурами, с наличием невыраженной зоны склероза вокруг опухоли. При локализации в области крестца характерно поражение нескольких позвонков, центральное расположение опухоли. Характерно истончение и вздутие кортикального слоя, возможно разрушение кортикального слоя опухолью с наличием экстраоссального компонента в полости малого таза. При локализации в верхнешейных позвонках и основании черепа остеолитический очаг вызывает разрушение костных элементов основания черепа, без четких границ, или тел позвонков с наличием истончения и вздутия кортикального слоя с увеличением тени предпозвоночных мягких тканей или появления дополнительного мягкотканного компонента в проекции носа и ротоглотки. При локализации опухоли в других отделах позвоночника очаг деструкции преимущественно располагается в области тел позвонков, вызывая истончение и вздутие кортикального слоя с увеличением слоя предпозвоночных мягких тканей. Возможен быстрый рост опухоли с появлением рентгенологических признаков злокачественного роста (разрушение кортикального слоя, отсутствие четких границ, быстро увеличивающийся экстраоссальный компонент).
Лечение хордомы хирургическое — радикальное удаление опухоли. При невозможности осуществить радикальное оперативное вмешательство показана с паллиативной целью лучевая терапия: с обезболивающей целью используется любая общепринятая методика.
Злокачественные опухоли костей
Остеосаркома
Является одной из наиболее частых и чрезвычайно злокачественных опухолей костей. По данным различных авторов, остеосаркома регистрируется в 30–80% всех сарком костей, а по статистике клиники Мейо, встречается в 2–8 раз чаще и по частоте уступает лишь миеломной болезни. Наиболее характерна заболеваемость во втором, реже — в третьем десятилетии жизни. Редко может встречаться и в более старшем возрасте, а в пожилом возрасте — чаще всего на фоне болезни Педжета. У лиц мужского пола опухоль встречается несколько чаще.
Клиника. Характерен выраженный болевой синдром, появляющийся с самых ранних стадий заболевания, усиливающийся по ночам. После приема анальгетиков, эффект незначительный, при приеме наркотиков боли снимаются лишь на время действия препарата. Локализуется опухоль чаще всего в метафизах длинных трубчатых костей, наиболее часто — в области коленного сустава, реже — в костях таза, но может поражать практически любую часть скелета. При осмотре выявляется увеличение объема (окружности) конечности над опухолью, усиление сосудистого рисунка, повышение местной температуры. Часто имеется ограничение движений в близлежащем суставе. Нередко наступают патологические переломы. Болезнь неуклонно прогрессирует (без ремиссий), характерен небольшой срок от начала заболевания до момента обращения к врачу.
Диагностика. Ведущим диагностическим методом, наряду с клиникой, является рентгенография. Характерно наличие очага деструкции кости, не имеющего четких контуров. Отсутствует зона склероза вокруг очага деструкции. Кортикальный слой кости разрушен. Сравнительно рано выявляется выход опухоли в окружающие мягкие ткани. Выделяются центральная и периферическая формы, а по характеру очага деструкции выделяют 3 формы: остеолитическая, остеобластическая и смешанная. Остеолитическая форма — бесструктурный очаг разрушения кости, остеобластическая форма — очаг деструкции с участками склероза и уплотнения, смешанная форма — сочетание участков остеолитической и остеобластической форм. Во всех случаях очаг деструкции не имеет четких контуров. Характерна периостальная реакция в виде козырька Кодмена или спикулообразного (игольчатого) периостита. В экстраоссальном компоненте опухоли возможны участки оссификации (патологическое костеобразование). На ранних стадиях заболевания опухоль может проявляться центрально или эксцентрически расположенным литическим очагом деструкции небольших размеров, с нечеткостью контуров кортикального слоя на ограниченном протяжении. Деструкция быстро нарастает и уже через 2–3 нед определяются вышеописанные типичные рентгенологические симптомы. Патологические переломы чаще наблюдаются при литических формах. Характерно ранее гематогенное метастазирование в легкие. Во всех случаях до начала лечения необходима морфологическая верификация опухоли. Материал для исследования получается при операционной или трепан-биопсии.
Патологическая анатомия. Остеосаркома отличается выраженным полиморфизмом с наличием большого количества митозов, с преобладанием при некоторых формах полиморфноклеточных или веретеноклеточных элементов. Обязательным признаком является наличие новообразованных остеоидных структур, от отдельных бесформенных полей остеоида до значительных очагов примитивного костеобразования. Встречается хондробластический вариант, который бывает трудно отличить от низкодифференцированной формы хондросаркомы.
Дифференциальный диагноз проводится с другими злокачественными опухолями костей (саркома Юинга, злокачественная фиброзная гистиоцитома, гигантоклеточная опухоль и др.), от которых остеосаркому отличает выраженность, непрерывность и быстрота нарастания болевого синдрома, а также быстрый рост опухоли и нарушение функции конечности. Саркома Юинга редко возникает в возрасте старше 20 лет и локализуется в метадиафизарном, а не в метафизарном отделе трубчатой кости. Другие злокачественные опухоли кости развиваются существенно медленнее остеосаркомы и редко встречаются в возрасте моложе 20–25 лет.
Симулировать остеосаркому могут некоторые формы хронических гематогенных остеомиелитов, а также некоторые формы посттравматических периоститов или посттравматических параоссальных гетеротопических оссификатов. У больных старше 40–45 лет дифференциальный диагноз необходимо проводить с метастатическим поражением костей.
Лечение. Любые локальные методы лечения, включая расширенные операции, не предупреждают гематогенного метастазирования, проявляющегося в короткие сроки после начала лечения у абсолютного числа больных.
Стандартным методом лечения остеосаркомы в настоящее время является неоадьювантный подход. До операции проводятся несколько (3–4) курсов индукционной химиотерапии. Ее роль при лечении локализованной формы заболевания обобщенно выглядит следующим образом: уменьшение размеров опухоли, предупреждение ее возможного рецидива при сохранных операциях и профилактика отдаленного метастазирования. Предоперационная химиотерапия проводится в следующем режиме:
1. Доксорубицин — 90 мг/м2 в течение 96 ч. Препарат вводится в центральную вену.
2. Цисплатин — 120 мг/м2 в виде 4-часовой в/а инфузии на 5 сутки курса химиотерапии. Обеспечивается гидратация не менее 3,5 л и форсированный маннитом диурез.
Частота выраженных токсических проявлений после проведения данного режима может достигать 40%. Наиболее значимые проявления — гематологическая и гастроинтестинальная токсичность. При развитии фебрильной нейтропении назначаются антибиотики широкого спектра действия, противогрибковые препараты, переливаются компоненты крови, вводятся гемостимулирующие факторы.
После курсов полихимиотерапии следует радикальное хирургическое лечение. При локализации опухоли в длинных трубчатых костях и небольших ее размерах могут производиться органосохраняющие операции в объеме резекции суставного конца или тотальное удаление длинной трубчатой кости с эндопротезированием (рис. 2). При опухолях с большим внекостным компонентом показана ампутация (экзартикуляция) на уровне вышерасположенного сегмента конечности. Для уточнения степени распространенности опухолевого процесса используются КТ и МРТ, а также планарная сцинтиграфия.
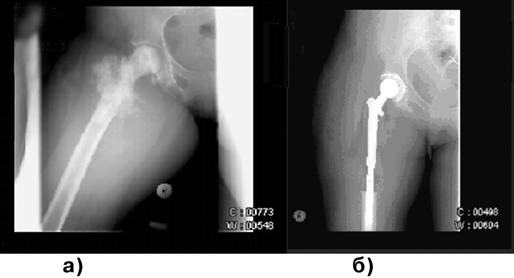
Рисунок 2. Остеосаркома бедренной кости:
а — до операции; б — после операции
Послеоперационная (адъювантная) химиотерапия определяется степенью лекарственного патоморфоза. При выраженном лечебном патоморфозе проводятся 3–4 курса теми же препаратами. При слабом гистологическом ответе — 6 курсов химиотерапии по схеме: этопозид — 100 мг/м2 в/в и ифосфамид — 1,8 г/м2 в/в в 1–5 дни.
Общая продолжительность лечения занимает около года, и проводить его следует предпочтительно в специализированных центрах, имеющих соответствующие возможности и опыт.
Указанный выше режим лечения позволяет достичь выраженного гистологического ответа (более 90% некроза опухоли) у 70% больных и выполнить органосохраняющие вмешательства в 80% случаев. Частота рецидивирования после хирургического лечения не превышает 10%.
Исход. 5-летняя выживаемость больных, леченных по современным методикам, достигает 70%.
Паростальная (юкстакортикальная) остеосаркома
Встречается довольно редко и составляет 2–5% всех злокачественных опухолей скелета, примерно с одинаковой частотой возникает как у мужчин, так и у женщин в возрасте от 15 до 75 лет.
Клиника. Заболевание начинается исподволь, чаще всего не вызывает болей. Опухоль характеризуется длительным течением (10–12 и более лет) до установления диагноза. Такое сравнительно спокойное по своим клиническим проявлениям течение процесса приводит к тому, что больные обращаются к врачу, когда опухоль, достигнув значительных размеров, вызывает боли или нарушает функцию близлежащего сустава. Но и на этом этапе часто общее состояние больного остается удовлетворительным. Такое торпидное течение дало основание некоторым авторам считать, что на определенном этапе своего развития опухоль доброкачественна. Но черты злокачественности, органически присущие этой опухоли, неизбежно проявляются в процессе ее роста склонностью к рецидивированию после нерадикально произведенных операций и метастазированию (преимущественно в легкие). Чаще опухоль локализуется в области метафиза или метадиафиза длинных трубчатых костей (дистальный метадиафиз бедренной и плечевой костей, реже большеберцовая кость). Опухоль пальпируется в виде костной плотности малоболезненного неподвижного по отношению к кости образования. Патологические переломы не описаны.
Диагностика. Рентгенологические изменения для этой опухоли очень характерны. Метафиз и близлежащая треть диафиза длинной трубчатой кости муфтообразно окутываются очень плотными костными массами. Наружный контур этой “муфты” полицикличен и чаще всего имеет четкие очертания. На рентгенограммах видно, что массив опухоли как бы образовался из отдельных “шаров” или “полушаров”, свободные края которых и создают резко полицикличный наружный контур — характерную картину, свойственную только паростальной саркоме. Рентгенологическая структура опухоли неравномерна. Хотя контуры костной ткани четко и интенсивно обозначены и имеется большая масса опухолевой ткани, деструкция самой кости и периостальная реакция отсутствуют или весьма слабо выражены. Представленные рентгенологические признаки ярко выражены у больных с достаточно запущенным процессом. В начальных же стадиях развития паростальной саркомы рентгенологическая диагностика может вызывать значительные трудности, в такой фазе развития ее нелегко дифференцировать с периферической хондросаркомой.
Патологическая анатомия. Микроскопически большинство паростальных сарком обнаруживают невысокую степень атипии. Кость морфологически выглядит достаточно зрелой, формирующей афункциональные костные балки. Фигуры митоза обнаруживаются в небольшом количестве. По периферии опухоли всегда имеется хрящ, по своему строению напоминающий хондросаркому, а при более агрессивном течении обнаруживается картина остеосаркомы. Микроскопическое исследование этой опухоли требует тщательности и кропотливости с просмотром многих ее отделов, а также изучения рентгеновской картины поражения. Характерной особенностью паростальной саркомы является ее инфильтрирующий рост, опухолевая ткань обхватывает нервные стволы и врастает в стенку магистральных сосудов.
Лечение. Хирургическое вмешательство является основным методом лечения. Частичное иссечение опухоли приводит к рецидиву процесса. Агрессивность же каждой последующей рецидивной опухоли нарастает. Паростальная саркома обладает способностью к аутотрансплантации, о чем свидетельствует рост опухоли в мягких тканях по ходу биопсийного канала с последующим образованием опухолевых узлов в обсемененных мягких тканях. Методом выбора считается резекция целого сегмента кости единым блоком с опухолью (для длинных трубчатых костей — резекция суставного конца) с пластическим замещением образовавшегося дефекта. В случаях, где такая операция радикально не может быть произведена, или у больных с рецидивом процесса после ранее произведенной операции, показана ампутация или экзартикуляция конечности. Лучевая терапия малоэффективна, химиотерапия на современном этапе не разработана.
Исходы лечения больных с этой опухолью несравненно лучше, чем для больных с остеосаркомой, и 5-летнее выздоровление составляет 60–70%. Частота рецидивирования при сохранных операциях — 45%, при калечащих — 10%.
Хондросаркома
Составляет около 10% первичных злокачественных опухолей костей и встречается в 2 раза чаще саркомы Юинга и в 2 раза реже остеосаркомы. По некоторым статистическим данным, хондросаркома наблюдается еще чаще (до 20% всех злокачественных опухолей костей). Различают первичную и вторичную хондросаркомы, последняя возникает в результате озлокачествления доброкачественных хрящевых опухолей или хрящевых дисплазий. Возникает в любом возрасте, но характерен средний возраст (40— 50 лет). Мужчины болеют в 1,5–2 раза чаще женщин. Частой локализацией первичной хондросаркомы являются кости конечностей, таза, и ребер. К редким локализациям хондросаркомы относят позвоночник и кости кисти.
Частота метастазирования зависит от степени анаплазии. При I степени (G1) она составляет 3%, при II (G2) — 32%, при низкодифференцированных хондросаркомах (III степень анаплазии — G3, мезенхимальная, дедифференцированная — G4) — 85%.
Клиника. Клинические проявления хондросаркомы зависят от особенностей морфологического строения. Для высокодифференцированных опухолей характерен длительный (4–5 лет) анамнез с малой выраженностью симптомов. Опухоли могут достигать больших размеров. Медленное, но неизменно завершающееся прогрессированием, развитие заболевания свойственно больным в возрасте старше 30 лет. При анаплазированных хонросаркомах (чаще у лиц молодого возраста) длительность симптомов не превышает 1–3 мес.
Основными клиническими проявлениями заболевания являются боли, припухлость. Боли отмечаются постоянством, прогрессивным нарастанием интенсивности. Увеличение размеров припухлости нередко идет месяцами, иногда годами, особенно при вторичных хондросаркомах. Другие местные симптомы, такие как расширение сети подкожных вен, местное повышение температуры, а также нарушение функции близлежащего сустава, выражены менее резко, чем при остеосаркоме или совсем отсутствуют. Лабораторные исследования не выявляют ничего характерного для хондросаркомы.
Рентегнологически хондросаркома характеризуется наличием центрально или эксцентрически расположенного очага деструкции остеолитического характера, чаще больших размеров, с нечеткими контурами и отсутствием зоны склероза. Характерны участки обызвествления в проекции очага деструкции кости. При эксцентрическом расположении опухоли или при увеличении размеров центрально расположенной хондросаркомы, наблюдается истончение, вздутие и разрушение кортикального слоя с проявлением экстраоссального компонента опухоли с участками обызвествления. Козырек Кодмена нехарактерен. Возможны слоистые и бахромчатые периостальные наслоения. Различают центральную хондросаркому (из внутренних отделов кости) и периферическую (из поверхностных слоев кости, врастающую в окружающие мягкие ткани). При развитии периферической, экстраоссального типа хондросаркомы кость может быть почти не изменена, а в прилежащих мягких тканях определяется добавочное образование. Нередко на фоне этой мягкотканной тени имеются очаги обызвествления, которые при КТ выявляются постоянно, что является характерным признаком для этой опухоли (рис. 3).
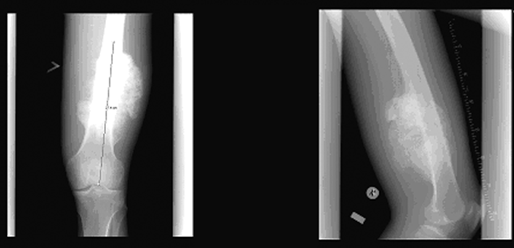
Рисунок 3. Рентгенологическая картина хондросаркомы бедренной кости
Патологическая анатомия. Патоморфологическая диагностика хондросарком в типично выраженных и далеко зашедших случаях обычно не представляет затруднений. Однако ткань опухоли имеет различную степень анаплазии. Еще одной особенностью хондросаркомы является ее способность прорастать в стенки магистральных сосудов. Определяющим диагностическим признаком хрящевой природы опухоли является межуточное вещество, количество и качество которого значительно варьирует.
Выраженный полиморфизм клеток с фигурами атипичных митозов при хондроидном характере межуточного вещества с участками некрозов и миксоматозного превращения не вызывает трудностей в постановке диагноза. Биопсию опухоли следует проводить так, чтобы очаг поражения, вместе с биопсийным раневым каналом, по ходу операции был убран целиком в пределах здоровой ткани без его вскрытия, чтобы рана не оказалась обсеменена опухолевыми клетками.
Описаны также мезенхимальная и дедифференцированная формы хондросаркомы, протекающие более злокачественно за счет ранней гематогенной диссеминации, а также светлоклеточная форма хондросаркомы, близкая по своему строению к хондробластоме. Наиболее характерные элементы гистологической картины — своеобразные “светлые” клетки, содержащие включения гликогена, а также многоядерные гигантские клетки.
Лечение. Основной метод лечения типичной хондросаркомы — радикальное оперативное удаление опухоли в пределах здоровых тканей. Чрезвычайно важным является абластичность проведения операции — удаление костной и мягкотканной опухоли единым блоком с запасом окружающих здоровых тканей, чтобы избежать попадания опухолевых клеток в рану. При отсутствии большого мягкотканного компонента опухоли показаны резекции суставных концов длинных трубчатых костей или их тотальное удаление с эндопротезированием дефекта. При локализации в лопатке и костях таза — межлопаточно-грудная и межподвздошно-брюшная резекции соответственно. При больших размерах опухоли — ампутация (экзартикуляция). Прогноз после радикальной операции при хондросаркоме благоприятен. Но удаление опухоли технически оказывается невозможным при некоторых ее локализациях, например, в позвоночнике. Лучевое лечение хондросарком дает лишь временный, паллиативный (обезболивающий) эффект.
При низкодифференцированных хондросаркомах (III степень анаплазии — G3, дедифференцированная, мезенхимальная — G4) используются протоколы неоадъювантной химиотерапии, применяемые для лечения остеосаркомы.
Исход лечения больных с хондросаркомой прямо коррелирует со степенью анаплазии этой опухоли. 5-летняя выживаемость при анаплазии I степени составляет 83%, при анаплазии II степени — 60%, при анаплазии III степени — 19%. При мезенхимальной хондросаркоме — 22%. При дедифференцированной хондросаркоме — 11%. Частота рецидивирования в зависимости от гистологического варианта опухоли и степени анаплазии колеблется от 8 до 28%.
Саркома Юинга
Саркома Юинга, а также ПНЭО и опухоль Аскина, выделенные в последние годы в отдельную группу первичных новообразований костей, относятся к редким злокачественным новообразованиям человека. Они встречаются преимущественно у лиц молодого возраста, характеризуются агрессивным течением и склонностью к ранней гематогенной диссеминации. Эти опухоли рано метастазирует в легкие, а также в другие кости скелета и регионарные лимфатические узлы.
Клиника. Возраст — наиболее часто второе десятилетие жизни, реже — третье. Мужчины болеют в 2 раза чаще, чем женщины. Опухоль локализуется преимущественно в диафизах длинных трубчатых костей, может локализоваться в плоских и коротких трубчатых костях. Характерно быстрое начало. Ранним и частым симптомом при саркоме Юинга являются боли. Они возникают у 80% больных. Боли носят периодический и даже волнообразный характер. Доминирующим и наиболее важным признаком болезни является выявление опухоли, которое удается уже при первичном осмотре, что подчеркивает тенденцию этой опухоли разрушать кортикальный слой и распространяться на окружающие мягкие ткани. Заболевание нередко начинается так, как это бывает при остеомиелите. Отмечаются подъемы температуры почти у половины больных, иногда до 38–39oC, повышение местной температуры, усиление сосудистого рисунка над опухолью, болезненность при пальпации, увеличение объема конечности, иногда гиперемия, возможна атрофия мышц. Часто выявляется умеренный лейкоцитоз. Симптомы обычно быстро нарастают, но наряду с быстрым и даже молниеносным течением у одних больных, у других отмечается более спокойное и длительное течение. Иногда отмечается волнообразное течение с периодами обострений и непродолжительными ремиссиями. Средняя длительность симптомов до обращения к врачу по данным нашей клиники — 26 нед. Наиболее короткий анамнез — 2 нед., наиболее продолжительный — 2 года. Важной биологической особенностью саркомы Юинга является ее высокая чувствительность к лучевому воздействию, что иногда используется в диагностических целях.
Рентгенологическая картина характеризуется мелкоочаговой деструкцией метадиафизарного отдела кости, без четких контуров, с отсутствием зоны склероза. Характерны разволокнение кортикального слоя (интракортикальная деструкция), слоистый периостит. При значительных размерах опухоли возможно разрушение кортикального слоя с появлением игольчатого периостита. В динамике в период ремиссии возможна ассимиляция луковичного периостита. При локализации в плоских костях, помимо мелкоочаговой деструкции, возможно реактивное костеобразование без четких контуров (рис. 4).
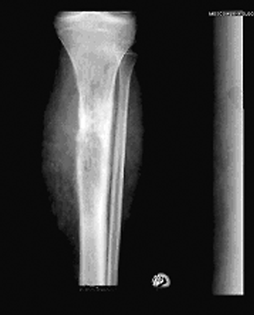
Рисунок 4. Рентгенологическая картина саркомы Юинга
Патологическая анатомия. Характерна в микроскопической картине однотипность ее округлых клеток, что отличает саркому Юинга от ретикулоклеточной саркомы. Иногда клетки располагаются в виде “псевдорозеток”, правильная сеть аргирофильных волокон отсутствует, нередко имеются полости, ограниченные непосредственно опухолевыми клетками, содержащие кровь.
Лечение больных саркомой Юинга и ПНЭО — комбинированное с обязательным использованием химиотерапии. Применяются следующие режимы:
VACA — винкристин — 1,5 мг/м2 в/в в 1 день, доксорубицин — по 20 мг/м2 в/в в 1–3 дни, циклофосфамид — 1200 мг/м2 в 1 день, дактиномицин — по 0,5 мг/м2 в 1–3 дни.
VAIA — винкристин — 1,5 мг/м2 в/в в 1 день, дактиномицин — по 0,5 мг/м2 в 1–3 дни, ифосфамид — по 2 г/м2 в 1–3 дни, доксорубицин — по 20 мг/м2 в/в в 1–3 дни.
VIDE — винкристин — 1,5 мг/м2 в/в в 1 день, ифосфамид — по 3 г/м2 в 1–3 дни, доксорубицин — по 20 мг/м2 в/в в 1–3 дни, этопозид — по 100 мг/м2 в 1–3 дни.
До локального лечения проводятся 4–6 курсов с интервалом 3 нед.
В настоящее время используются лучевой, хирургический и комбинированный методы локального лечения. Современные режимы индукционной химиотерапии позволяют выполнить в большинстве случаев органосохраняющие операции в объеме резекции или тотального удаления пораженной кости. Многие исследователи сходятся во мнении, что наиболее надежным локальный контроль опухоли бывает при проведении лучевой терапии после радикального хирургического лечения.
После операции проводятся курсы поддерживающей полихимиотерапии. Таким образом лечение саркомы Юинга длится около 1 года.
Исход. Современные методы лечения обусловливают достоверное увеличение процента выживших 5 и более лет — до 60 и даже 80%. Частота рецидивирования доходит до 26% при лучевом методе и не превышает 10% при сочетании химиотерапии с лучевой терапией и оперативным вмешательством.
Фибросаркома кости
Встречается редко (1–4% всех костных опухолей), наиболее часто в 20–40 лет (средний возраст — 32 года, по данным нашей клиники). До 70% случаев локализуется в костях, формирующих коленный сустав. Боль средней интенсивности, медленно прогрессирующая, усиливающаяся к ночи, локальная, купируется наркотическими анальгетиками. Видимая причина отсутствует, эффект от лечения отсутствует или кратковременный (неспецифическое лечение). Длительность заболевания до обращения к врачу — более 6 мес (медленное течение). Часто определяется изменение контура крупного сустава или наличие опухолевидного образования, неподвижного относительно кости. Встречаются патологические переломы (10%).
Рентгенологически фибросаркома кости локализуется в суставных концах трубчатых костей (метадиафизы), по преимуществу — в области коленного сустава. Очаг деструкции, как правило, имеет центральное расположение, форма неправильная, контуры нечеткие, зона склероза отсутствует. Характер очага, как правило, остеолитический, обызвествления отсутствуют или неявно выражены, возможно наличие козырька Кодмена, разрушение кортикального слоя. Динамика отрицательная. В отличие от остеогенной саркомы, не бывает игольчатого периостита. Может иметь место патологический перелом, который не срастается. Выделяют периферическую форму фибросаркомы, при которой преимущественно поражается кортикальный слой и окружающие мягкие ткани. Характерно пальпируемое опухолевидное образование. Окончательный диагноз выставляется при гистологическом исследовании.
Лечение. Опухоль не чувствительна к лучевой и химиотерапии. Лечение хирургическое. При начальных стадиях опухоли показаны органосохраняющие операции: резекция суставного конца длинной трубчатой кости с эндопротезированием, межлопаточно-грудная или межподвздошно-брюшная резекции и др. При больших размерах опухоли — ампутации и экзартикуляции.
Злокачественная фиброзная гистиоцитома (ЗФГ)
До недавнего времени ЗФГ считалась редким заболеванием. В последние десятилетия публикуются наблюдения над десятками больных с диагнозом ЗФГ, которые обследовались и лечились в одном учреждении за сравнительно короткий отрезок времени. Возможно, что частота диагноза ЗФГ является данью времени и в эту группу включается ряд больных с гигантоклеточной опухолью, фибросаркомой или другими опухолями костей и мягких тканей, структурно близких к ЗФГ.
Первичная ЗФГ составляет около 3% от всех злокачественных костных опухолей. По некоторых данным среди больных старше 40 лет ЗФГ — самая частая опухоль.
Клиника. Основными симптомами первичной ЗФГ являются боли, клинически выявляемое опухолевое образование. Почти у половины больных эти основные признаки появляются одновременно. ЗФГ кости чаще всего локализуется в нижнем отделе бедренной и верхнем — большеберцовой кости. Обычно анамнеза длится от 1 до 12 мес, но половина больных обращается в первый месяц (начало заболевания).
На рентгенограммах выявляется центрально или эксцентрично расположенный очаг деструкции, чаще литического типа. Часто выявляется разрушение кортикального слоя. По данным некоторых авторов, различные типы периостальной реакции фиксируются более чем у 80% больных, тогда как другие отмечают сравнительно редкую реакцию надкостницы в виде линейного периостита. По данным ГУ РОНЦ им. Н.Н. Блохина РАМН, у каждого четвертого больного наступал патологический перелом, а у 2/3 больных выявлялись метастазы (у всех в легкие, а у нескольких пациентов — в регионарные лимфатические узлы). По другим данным, метастазы в регионарные лимфатические узлы регистрировались у 16% леченных пациентов.
Патологическая анатомия. ЗФГ является двухкомпонентной опухолью. Ее основными клеточными элементами, выявляемыми как при световой, так и при электронной микроскопии, являются гистиоцитоподобные и фибробластоподобные клетки, среди которых могут встречаться многоядерные и ксантомные клетки, а также блуждающие клетки стремы. Некоторые авторы, однако, высказывают сомнение в том, что эту опухоль следует расценивать как самостоятельную нозологическую форму. Теоретически рассматриваются три основных источника развития ЗФГ:
1. Опухоль развивается из гистиоцитов (гистиоцитарная теория).
2. Опухоль развивается из плюрипотентных мезенхимальных стволовых клеток, которые в процессе дифференцировки и роста опухоли формируют как гистиоцитоподобные, так и фибробластоподобные клеточные элементы, но в постнатальном периоде их развитие идет независимым путем (плюрипотентная теория).
3. Опухоль формируют фибробласты, которые в процессе опухолевого роста приобретают свойства гистиоцитов (фибробластическая теория).
В настоящее время ни одна из этих теорий не может считаться доказанной.
Лечение. ЗФГ относится к опухолям высокого злокачественного потенциала. Для лечения данной опухоли используются неоадьювантные протоколы, как для остеосаркомы. Стандартным методом локального лечения является хирургический, при этом соблюдаются те же принципы и виды оперативных вмешательств, как и при остеосаркоме.
Исход. 5-летняя выживаемость при современных режимах комбинированного лечения составляет около 50%.
Литература
Азизов М.Ж. и др. ...Вертебрология — проблемы, поиски, решения: Научная конференция. 27–29 мая 1998 г., Москва.— М., 1998.— С. 207–208.
Алиев М.Д. Медико-социальная реабилитация больных, перенесших радикальное лечение по поводу опухолей опорно-двигительного аппарата.— М., 1992.— 297 с.
Алиев М.Д. и др. ...Вопр. онкологии.— 1999.— № 3.— С. 317–320.
Анисеня И.И. ...Опухоли мягких тканей: Тезисы Межгосударственного симпозиума. 9–10 сентября 1992 г., Ярославль.— Спб., 1992.— С. 4–5.
Ардашев И.П. ...Ортопед., травматол. и протезирование.— 1991.— № 2.— С. 68–72.
Ардашев И.П. и др. ...Хирургия позвоночника и спинного мозга.— Новокузнецк, 1995.— С. 19–24.
Бабкин А.В. и др. ...Вертебрология — проблемы, поиски, решения: Научная конференция. 27–29 мая 1998 г., Москва.— М, 1998.— С. 212–213.
Брайцев В.Р. Фиброзная дисплазия.— М., 1947.
Бублик Л.А. и др. ...Вертебрология — проблемы, поиски, решения: Научная конференция. 27–29 мая 1998 г., Москва.— М., 1998.— С. 221–222.
Бурдыгин В.Н. и др. ...Удаление конечностей и замещение дефектов костей.— Ялта, 1996.— С. 27–28.
Бурдыгин В.Н. и др. ...Вест. травматол. и ортопедии.— 1998.— № 1.— С. 3–12.
Виноградова Т.Н. Опухоли костей.— М.: Медицина, 1973.
Волков М.В. Болезни костей у детей.— М.: Медицина, 1985.
Вреден Р.Р. Злокачественные опухоли костей/Под ред. Н.Н. Петрова.— 1934. — Т. 2.
Зацепин С.Т. Сохранные операции при опухолях костей.— М.: Медицина, 1984.— 288 с.
Кныш И.Т. и др. Первичные опухоли таза.— Киев: Здоровье, 1989.
Ковбасенко Л.А. ...Ортопед., травматол. и протезирование.— 1991.— № 3.— С. 72–73.
Краевский Н.А. и др. К патогенезу остеогенной саркомы//Опухоли опорно-двигательного аппарата.— 1971.— Вып. 3.— № 14.— С. 51–56.
Краевский Н.А. и др. ...Материалы пленума правления Всесоюзного общества онкологов.— М., 1974.— С. 134–135.
Кузьмина Л.А. ...Остеобластокластома.— М., 1962.— С. 70–73.
Лагунова И.Г. Клинико-рентгенологическая диагностика дисплазий скелета.— М.: Медицина, 1989.
Махсон А.Н. ...Вест. травматол. и ортопедии.— 1998.— № 1.— С. 17–20.
Махсон Н.Е. и др. Адекватная хирургия при опухолях плечевого и тазового пояса.— М., 1998.
Проценко А.И. и др. ...Вестн. травматол. и ортопедии.— 2000.— № 1.— С. 22–25.
Томита К. и др. ...Вестн. травматол. и ортопедии.— 1996.— № 2.— С. 11–18.
Трапезников Н.Н. и др. Опухоли костей.— М.: Медицина, 1986.
Abdu W.A. et al. ...Spine.— 1998.— V. 23 (24).— P. 2767–2777.
Day G.A. et al. ...Bull. Hosp. Jt. Dis.— 1998.— V. 57 (1).— P. 11–15.
Enneking W.F. ...J. Bone Jt. Surg.— 1966.— V. 48A.— P. 991–1007.
Formica C. et al. ...Chir. Organi Mov.— 1998.— V. 83 (1–2).— P. 23–33.
Lichtenstein L. Bone Tumors.–1997.
Putman M.D. et al. ...Hand-Clin.— 1995.— V. 11 (2).— P. 265–286.
Sridhar R. et al. ...Br. J. Neurosurg.— 1998.— V.12 (5).— P. 430–433.
Sundaresan N. et al. ...Neurosurg. Clin. N. Am.— V. 8 (4).— P. 541–543.
Unni K.K. ...Cancer.— 1976.— V. 37 (5).— P. 2466–2475.
Описание проверено экспертом
Оцените статью:
- Опухоли костей злокачественные
- Опухоли костей и суставов
Полужирным шрифтом выделены лекарства, входящие в справочники текущего года. Рядом с названием препарата может быть указан ежегодный уровень индекса информационного спроса (показатель, который отражает степень интереса потребителей к информации о лекарстве).
новообразование костей
опухоли позвоночника, опухоль позвоночника,



